Questões Sobre Termologia - Física - concurso
1701) Em 1962, um jingle (vinheta musical) criado por Heitor Carillo fez tanto sucesso que extrapolou as fronteiras do rádio e chegou à televisão ilustrado por um desenho animado. Nele, uma pessoa respondia ao fantasma que batia em sua porta, personificando o “frio”, que não o deixaria entrar, pois não abriria a porta e compraria lãs e cobertores para aquecer sua casa. Apesar de memorável, tal comercial televisivo continha incorreções a respeito de conceitos físicos relativos à calorimetria.
- A) Aquecer a casa e os corpos.
- B) Evitar a entrada do frio na casa e nos corpos.
- C) Minimizar a perda de calor pela casa e pelos corpos.
- D) Diminuir a entrada do frio na casa e aquecer os corpos.
- E) Aquecer a casa e reduzir a perda de calor pelos corpos.
A resposta certa é a letra C) Minimizar a perda de calor pela casa e pelos corpos.
Essa alternativa está correta porque o comercial televisivo em questão promove a compra de luvas e cobertores para se aquecer em casa. No entanto, há um erro conceitual, pois a pessoa não deixa o fantasma (que representa o frio) entrar em casa, mas, ao mesmo tempo, não abre a porta para comprar luvas e cobertores. Isso é incorreto, pois a porta é aberta para que o calor entre e o frio seja mantido do lado de fora.
Assim, a alternativa C) é a mais adequada, pois minimizar a perda de calor pela casa e pelos corpos é o objetivo principal do comercial. Ao fechar a porta e usar luvas e cobertores, a pessoa está evitando que o calor escape e, simultaneamente, mantendo o frio do lado de fora.
É importante notar que as demais alternativas não são completamente corretas. A alternativa A) está incorreta, pois o objetivo não é apenas aquecer a casa e os corpos. A alternativa B) está errada, pois evitar a entrada do frio na casa e nos corpos não é o objetivo principal do comercial. A alternativa D) também está incorreta, pois diminuir a entrada do frio na casa e aquecer os corpos não é o foco do comercial.
Em resumo, a alternativa C) é a mais adequada, pois minimizar a perda de calor pela casa e pelos corpos é o objetivo principal do comercial, e fechar a porta e usar luvas e cobertores são maneiras de alcançar esse objetivo.
1702) Uma compressa contém 200 g de gelo à temperatura de 0 ,ºC. Se uma fonte transmite calor a essa compressa a uma taxa de 3,33, kJ/min, onde 1 ,kJ = 103,J, em quanto tempo todo o gelo se derreterá, com a temperatura final permanecendo em 0, ºC? Dado: calor latente de fusão do gelo L = 333 , kJ/kg.
- A) 5,0 min
- B) 10 min
- C) 15 min
- D) 20 min
- E) 25 min
A alternativa correta é letra D) 20 min
Gabarito: D
Primeiramente, vamos calcular a quantidade de calor para derreter todo o gelo, utilizando a equação do calor latente:
Q = mL
De acordo com o enunciado, temos que m = 200 , g = 0,2 , kg. Logo,
Q = 0,2 cancel {kg} cdot 333 dfrac { kJ } { cancel {kg} }
Q = 66,6 , kJ
Sabendo a taxa que a fonte de calor transmite para a compressa, podemos calcular o intervalo de tempo da seguinte maneira:
P = dfrac Q { Delta t }
Logo,
3,33 dfrac { cancel {kJ} } { min } = dfrac { 66,6 cancel {kJ} } { Delta t }
Delta t = 20 , min
Portanto, a resposta correta é a alternativa (D).
1703) Os dados sobre a informação nutricional indicam que um copo de 200 mL de certo refrigerante dietético possui 4,0 kcal, onde 1 kcal = 10^3 cal. Se toda esta quantidade de energia fosse fornecida na forma de calor a 500 gramas de água, em quantos graus a temperatura da água se elevaria? Dado: calor específico da água = 1,0 cal/g.°C.
- A) 1,0 °C
- B) 4,0 °C
- C) 8,0 °C
- D) 20 °C
- E) 50 °C
A alternativa correta é letra C) 8,0 °C
Gabarito: C
Os dados sobre a informação nutricional indicam que um copo de 200 mL de certo refrigerante dietético possui 4,0 kcal, onde 1 kcal = 10^3 cal. Se toda esta quantidade de energia fosse fornecida na forma de calor a 500 gramas de água, em quantos graus a temperatura da água se elevaria? Dado: calor específico da água = 1,0 cal/g.°C.
Resolução:
Para resolver essa questão, devemos lembrar que o calor sensível, que é utilizado para variar a temperatura de uma substância, é dado por:
Q = m c Delta theta tag 1
Onde m é a massa da substância, c é seu calor específico e Delta theta é a variação da temperatura.
De acordo com o enunciado, o copo de refrigerante possui 4,0 kcal. Como 1 kcal = 10^3 cal, podemos afirmar que a energia na forma de calor fornecida é Q = 4 times 10^3 , cal. Então, para uma massa de água m = 500 , g, a equação (1) se torna:
4 times 10^3 cancel {cal} = 500 cancel g cdot 1,0 dfrac { cancel {cal} } { cancel g °C } Delta theta
Delta theta = dfrac { 4 times 10^3 } { 500 } °C
Delta theta = 8 °C
Portanto, a resposta correta é a alternativa (c) 8,0 °C.
1704) No verão, várias cidades brasileiras atingem um nível de umidade relativa do ar inferior a 30%. Esta situação é particularmente prejudicial para crianças e idosos.
- A) 1,0 h
- B) 2,0 h
- C) 3,0 h
- D) 4,0 h
- E) 5,0 h
A alternativa correta é letra E) 5,0 h
Gabarito: E
No verão, várias cidades brasileiras atingem um nível de umidade relativa do ar inferior a 30%. Esta situação é particularmente prejudicial para crianças e idosos.
Para minimizar os efeitos da baixa umidade relativa do ar, pessoas utilizam vaporizadores de água para aumentar a umidade do ambiente. Certo vaporizador tem capacidade para 4,5 L de água. Sabendo que este vaporizador tem potência elétrica de 500 W, calcule por quanto tempo ele produzirá vapor quando ligado inicialmente com a sua capacidade máxima de água. Despreze o tempo que o vaporizador leva para aquecer a água da temperatura ambiente até 100 oC.
Dados: calor latente de vaporização da água Lv = 2000 kJ/kg; densidade da água dA = 1000 kg/m3; 1 L = 10−3 m3.
Resolução:
Sabemos que a potência de um aparelho é dada pela energia consumida por unidade de tempo, ou seja,
P = dfrac E { Delta t }
Portanto, sabendo a potência do vaporizador, devemos encontrar a quantidade de energia consumida pelo aparelho. Como essa energia será usada para vaporizar a água, desprezando-se as perdas, podemos afirmar que a energia E corresponde à quantidade de calor necessária para se vaporizar toda a água que está armazenada nele. Então, a equação acima se torna:
P = dfrac { Q_{latente} } { Delta t }
Lembrando que o calor latente é dado por Q_{latente} = mL, onde m é a massa e L é o calor latente, temos que:
Q_{latente} = m_A cdot L_v
Sendo v o volume de água e dA sua densidade, temos que:
Q_{latente} = v cdot d_A cdot L_v
Como dA = 1000 kg/m3 e 1 L = 10−3 m3, a massa de água é dada por
Q_{latente} = 4,5 cancel L cdot dfrac { 10^{-3} cancel {m^3 } } { cancel L } cdot dfrac { 1000 cancel {kg} } { cancel {m^3 } } cdot dfrac { 2.000 kJ } { cancel { kg} }
Q_{latente} = 9.000 , kJ
Então, o tempo que ele produzirá vapor quando ligado inicialmente com a sua capacidade máxima de água é dado por:
Delta t = dfrac { Q_{latente} } { P }
Delta t = dfrac { 9 times 10^3 cancel J } { 500 cancel J /s }
Delta t = 18.000 , s
Logo,
Delta t = 18.000 cancel s cdot dfrac { 1 cancel {min} } { 60 cancel s } cdot dfrac { 1 , h } { 60 cancel {min} }
Delta t = 5,0 , h
Portanto, a resposta correta é a alternativa (e) 5,0 h.
Questão 1705
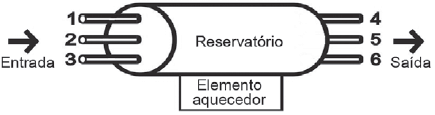
A configuração mais eficiente para a instalação dos pontos de entrada e saída de água no reservatório é, respectivamente, nas posições
- A) 1 e 4.
- B) 1 e 6.
- C) 2 e 5.
- D) 3 e 4.
- E) 3 e 5.
A resposta correta é a letra D) 3 e 4.
Para entender por que essa é a configuração mais eficiente, vamos analisar como funciona o sistema de aquecimento. A água fria entra no reservatório e é aquecida na base. Em seguida, a água quente é distribuída para as torneiras.
Quando a água fria entra pelo ponto 3 e a água quente sai pelo ponto 4, isso significa que a água quente está sendo distribuída para as torneiras a partir da região mais quente do reservatório. Isso é mais eficiente porque a água quente não precisa percorrer todo o caminho até a parte superior do reservatório para ser distribuída. Além disso, a água fria entra diretamente na região mais fria do reservatório, o que ajuda a reduzir a perda de calor.
Já nas outras configurações, a água quente precisa percorrer um caminho maior para ser distribuída, o que aumenta a perda de calor e reduz a eficiência do sistema. Além disso, a água fria pode entrar em contato com a água quente, o que também pode reduzir a eficiência do sistema.
Portanto, a configuração mais eficiente é a que minimiza a perda de calor e maximiza a eficiência do sistema de aquecimento, que é a configuração em que a água fria entra pelo ponto 3 e a água quente sai pelo ponto 4.
1706) Com base nas afirmativas a seguir em relação aos conceitos de calor e temperatura:
- A) I.
- B) II.
- C) III.
- D) I e II.
- E) I e III.
A resposta correta é a letra E) I e III.
Para entender por quê, resposta é essa, vamos analisar cada afirmação:
I - Calor é a energia que se transfere de um corpo para outro, quando existe diferença de temperatura entre eles.
Essa afirmação está correta. O calor é uma forma de energia que se transfere de um corpo para outro devido à diferença de temperatura entre eles. Isso ocorre porque as moléculas dos corpos em contato estão em movimento, e o movimento mais rápido das moléculas do corpo mais quente transfere energia para as moléculas do corpo mais frio.
II - Calor e temperatura representam o mesmo conceito físico.
Essa afirmação está incorreta. Embora o calor e a temperatura estejam relacionados, eles não representam o mesmo conceito físico. A temperatura é uma medida da energia cinética de agitação das moléculas de um corpo, enquanto o calor é a energia que se transfere de um corpo para outro devido à diferença de temperatura entre eles.
III - A temperatura de um gás está relacionada com a energia cinética de agitação de suas moléculas.
Essa afirmação está correta. A temperatura de um gás é uma medida da energia cinética de agitação de suas moléculas. Quanto maior a temperatura, mais rápido as moléculas se movem e mais alta é a energia cinética de agitação.
Portanto, as afirmações I e III estão corretas, e a afirmação II está incorreta.
1707) Em regiões mais frias, é usual utilizar o parâmetro “Sensação Térmica” para definir a temperatura percebida pelas pessoas. A exposição da pele ao vento é uma das variáveis que compõem esse parâmetro. Se durante essa exposição, a camada de ar em contato com a pele é constantemente renovada por outra com uma temperatura menor do que a pele, pode-se afirmar corretamente que
- A) não há troca de calor entre a pele e a camada de ar.
- B) há troca constante de calor da camada de ar para a pele.
- C) há troca constante de calor da pele para a camada de ar.
- D) há troca constante de calor da pele para camada de ar e vice-versa.
A alternativa correta é letra C) há troca constante de calor da pele para a camada de ar.
Gabarito: C
Em regiões mais frias, é usual utilizar o parâmetro “Sensação Térmica” para definir a temperatura percebida pelas pessoas. A exposição da pele ao vento é uma das variáveis que compõem esse parâmetro. Se durante essa exposição, a camada de ar em contato com a pele é constantemente renovada por outra com uma temperatura menor do que a pele, pode-se afirmar corretamente que
Resolução:
De acordo com a lei zero da termodinâmica, o calor somente flui de um corpo para outro quando não há equilíbrio térmico entre eles, ou seja, só há transferência de calor quando os corpos se encontram a temperaturas diferentes. Assim, como a pele está exposta à massa de ar a uma temperatura diferente, há troca de calor entre a pele e o ar. Como essa camada de ar em contato com a pele é constantemente renovada, essa troca é constante.
Além disso, de acordo com a segunda lei da termodinâmica e utilizando-se o enunciado de Clausius, podemos afirmar que que o calor flui espontaneamente de um corpo de temperatura mais alta para um corpo de temperatura menor. Nesse caso, o fluxo de calor tem sentido da pele para a camada de ar, já que o ar está a uma temperatura menor do que a pele.
Portanto, a resposta correta é a alternativa (C).
1708) Um caminhão, utilizado no abastecimento de aviões, recebe em seu reservatório a quantidade exata de combustível, medida em quilogramas, necessária para um avião realizar um voo. Essa quantidade de combustível, logo após ser colocado no reservatório do caminhão, tem exatamente o mesmo volume do reservatório do avião. Até chegar ao avião, o combustível, dentro do reservatório do caminhão, sofre uma dilatação volumétrica sem transbordar.
- A) a densidade do combustível, com a dilatação, não se altera
- B) a quantidade de combustível, em quilogramas, colocada no avião é maior
- C) o avião conseguirá completar o voo
- D) a quantidade de combustível, em quilogramas, é menor
A alternativa correta é letra D) a quantidade de combustível, em quilogramas, é menor
Gabarito: D
Um caminhão, utilizado no abastecimento de aviões, recebe em seu reservatório a quantidade exata de combustível, medida em quilogramas, necessária para um avião realizar um voo. Essa quantidade de combustível, logo após ser colocado no reservatório do caminhão, tem exatamente o mesmo volume do reservatório do avião. Até chegar ao avião, o combustível, dentro do reservatório do caminhão, sofre uma dilatação volumétrica sem transbordar.
Não percebendo a dilatação, o responsável realiza o abastecimento apenas se preocupando em preencher todo o volume do reservatório do avião. Podemos afirmar corretamente que
a) a densidade do combustível, com a dilatação, não se altera. INCORRETA.
Sabemos que a densidade é razão entre a massa e o volume, ou seja:
d = dfrac m V
Devido à alteração da temperatura, o volume de combustível sofreu alteração, mas a sua massa se manteve constante. Como a densidade e o volume são inversamente proporcionais, um aumento no volume implica na diminuição de densidade. Logo, a densidade do combustível, devido à dilatação, se alterou. Alternativa incorreta.
b) a quantidade de combustível, em quilogramas, colocada no avião é maior. INCORRETA.
Antes de ser colocado no reservatório do caminhão, a quantidade de combustível recebida tinha o mesmo volume do reservatório do avião. Devido à dilatação volumétrica, essa quantidade de combustível passa a ocupar um volume maior do que o reservatório do avião. Dessa forma, quando o reservatório do avião estiver cheio, ainda sobrará combustível no caminhão. Logo, a quantidade de combustível, em quilogramas, colocada no avião é menor. Alternativa incorreta.
c) o avião conseguirá completar o voo. INCORRETA.
Como mencionamos na alternativa (b), a quantidade de combustível em massa presente no reservatório do avião é menor do que a quantidade recebida pelo caminhão. Como essa quantidade é menor do que a necessária para o avião realizar o voo, o avião NÃO conseguirá completar o voo. Alternativa incorreta.
d) a quantidade de combustível, em quilogramas, é menor. CORRETA.
Como mencionamos na alternativa (b), a quantidade de combustível em massa presente no reservatório do avião é menor do que a quantidade recebida pelo caminhão. Alternativa correta.
Portanto, a resposta correta é a alternativa (D).
1709) Em um recente trabalho, os pesquisadores de uma instituição concluíram que 500 mL do total de água pura utilizada durante o processo de fabricação de um copo plástico são “perdidos” devido a mudança do estado líquido para o estado de vapor a 100 °C.
- A) 270
- B) 307,5
- C) 270000
- D) 307500
A alternativa correta é letra D) 307500
Gabarito: D
Em um recente trabalho, os pesquisadores de uma instituição concluíram que 500 mL do total de água pura utilizada durante o processo de fabricação de um copo plástico são “perdidos” devido a mudança do estado líquido para o estado de vapor a 100 °C.
Em termos de energia, essa quantidade de água pura “perdida” equivale, em calorias, a ____.
Considere:
1 – que a água pura, antes de entrar no processo de fabricação, está a 25 °C;
2 – calor específico da água pura igual a 1 cal/g°C;
3 – calor latente de vaporização da água pura igual a 540 cal/g; e
4 – a densidade da água pura igual a 1 g/cm³.
Resolução:
O calor total perdido nesse processo consiste no calor Q_1 necessário para elevar a temperatura de 500 ml de água de 25°C até 100°C, somado ao calor Q_2 necessário para evaporar essa mesma quantidade de água. Então, podemos calcular Q_1 da seguinte maneira:
Q_1 = m c Delta theta
Como a densidade da água pura igual a 1 g/cm³ e 1ml = 1 cm3, temos que m = 500 , g, c = 1,0 , cal /g°C e Delta theta = 100°C - 25°C = 75°C. Assim, a equação acima se torna:
Q_1 = 500 cdot 1 cdot 75
Q_1 = 37500 , cal
Agora, vamos calcular o calor necessário perdido na mudança do estado líquido para o estado de vapor:
Q_2 = m L
Q_2 = 500 cdot 540
Q_2 = 270000 , cal
Então, temos que:
Q_{total} = Q_1 + Q_2 = 37500 + 270000
Q_{total} = 307500 , cal
Portanto, a resposta correta é a alternativa (D).
1710) Um sistema de arrefecimento deve manter a temperatura do motor de um carro em um valor adequado para o bom funcionamento do mesmo. Em um desses sistemas é utilizado um líquido de densidade igual a 103 kg/m3 e calor específico igual a 4200 J/kg °C. Durante a troca de calor, o volume do líquido em contato com o motor é de 0,4 × 10-3 m3, a cada segundo, e a temperatura inicial e final do líquido é, respectivamente, igual a 80°C e 95°C. Considerando que esse volume de líquido está em
- A) 42000
- B) 25200
- C) 4200
- D) 2520
A alternativa correta é letra B) 25200
1º PASSO - Calcular o valor da massa a partir da fórmula de densidade:
d=frac{m}{V}
10^{3}=frac{m}{4.10^{-4}}
m=4.10^{-1}~kg
2º PASSO - Aplicar a fórmula de quantidade de calor:
Q=m.c. Delta t
Q=0,4.4200. left( 95-80 right)
Q=25200 J
3º PASSO - Calcular a potência (considerando o tempo de 1 segundo)
Pot=frac{Q}{t}
Pot=frac{25200~J}{text{1 s}}
Pot=25200 W
