Questões Sobre Termologia - Física - concurso
1711) Uma esfera homogênea de raio R, cuja densidade é de 2,7g/ cm^3 e o calor específico vale 0,2 callgºC, está a uma temperatura de -100ºC. Coloca-se essa esfera em um reservatório, isolado termicamente e de capacidade térmica desprezível, que contém 0,1 litro de água a 0ºC. Qual o valor mínimo de R, em centímetros, para que toda a água congele?
- A) 8,4
- B) 6,2
- C) 4,7
- D) 3,3
- E) 1,5
A alternativa correta é letra D) 3,3
Gabarito: D
Uma esfera homogênea de raio R, cuja densidade é de 2,7g/ cm^3 e o calor específico vale 0,2 cal/gºC, está a uma temperatura de -100ºC. Coloca-se essa esfera em um reservatório, isolado termicamente e de capacidade térmica desprezível, que contém 0,1 litro de água a 0ºC. Qual o valor mínimo de R, em centímetros, para que toda a água congele?
Dados: massa específica da água = 1,0 g/cm³
calor latente de fusão da água = 80 cal/g.
Resolução:
Primeiramente, vamos calcular a quantidade de calor necessária para congelar 0,1 litro de água a 0°C utilizando a equação do calor latente:
Q = mL
Lembrando que, para água, 0,1 l = 0,1 kg = 100 g, Logo,
Q = 100 cancel g cdot 80 dfrac { cal } { cancel g }
Q = 8.000 , cal
Agora, utilizando a equação do calor sensível, vamos calcular a massa da esfera que será capaz de fornecer essa quantidade de calor ao variar sua temperatura em 100°C ( de -100°C até 0°C):
Q = m c Delta theta
8.000 cancel {cal} = m cdot 0,2 dfrac { cancel {cal} } { g cancel {°C } } cdot 100 cancel {°C }
m = 400 , g
Sabendo a massa m e a densidade rho da esfera, podemos calcular o seu volume:
v = dfrac { m } { rho }
Logo,
v = dfrac { 400 cancel g } { 2,7 cancel g / cm^3 }
v = dfrac { 400 } { 2,7 }cm^3
Entretanto, sendo R o valor do raio da esfera, temos que:
v = dfrac { 4 pi R^3 } 3 = dfrac { 400 } { 2,7 }cm^3
Logo,
R^3 = dfrac { 3 cdot 400 } { 2,7 cdot 4 pi }cm^3
Para facilitar os cálculos a fim de encontrar a alternativa correta, vamos usar pi approx 3. Logo,
R^3 = dfrac { cancel 3 cdot {cancel {400}}^{100} } { 2,7 cdot cancel 4 cancel pi }cm^3
R^3 = dfrac { 100 } { 2,7 }cm^3
R^3 = dfrac { 1000 } { 27 }cm^3
R = sqrt[3]{ dfrac { 1000 } { 27 }cm^3 }
R = dfrac { 10 } { 3 } cm
R = 3,33 , cm
Portanto, a resposta correta é a alternativa (d) 3,3.
1712) Em relação aos conceitos de mecânica, hidrostática e termologia, assinale a opção correta.
- A) . A transferência de calor por condução e convecção é possível através do vácuo.
- B) Quando uma pessoa toca com o dedo em um bloco de gelo, o frio flui do gelo para a pessoa.
- C) Ao tocar em uma porta de madeira e em sua maçaneta de metal uma pessoa nota diferentes sensações térmicas, por exemplo que a maçaneta está mais fria do que a porta.
- D) A energia potencial gravitacional depende da escolha do referencial adotado.
- E) O módulo do empuxo exercido por um liquido sobre um corpo totalmente submerso nesse liquido é sempre igual ao módulo do peso do corpo.
ESTA QUESTÃO FOI ANULADA, NÃO POSSUI ALTERNATIVA CORRETA
Gabarito: anulada
Em relação aos conceitos de mecânica, hidrostática e termologia, assinale a opção correta.
a) A transferência de calor por condução e convecção é possível através do vácuo. INCORRETA.
Na condução, o calor é transferido pelo contato direto entre dois corpos de diferentes temperaturas. Na convecção, a transferência de calor acontece graças ao movimento de correntes de fluido devido à diferença de temperatura, como pode ser observado na formação das brisas marítimas e terrestres. Nesse dois casos, deve haver matéria para que haja transferência de calor, ou seja, não ocorrem no vácuo. Alternativa incorreta.
b) Quando uma pessoa toca com o dedo em um bloco de gelo, o frio flui do gelo para a pessoa. INCORRETA.
Espontaneamente, o calor flui no sentido do corpo mais quente para o mais frio, e não o contrário. Logo, quando uma pessoa toca com o dedo em um bloco de gelo, o frio flui da pessoa para o gelo. Alternativa incorreta.
c) Ao tocar em uma porta de madeira e em sua maçaneta de metal uma pessoa nota diferentes sensações térmicas, por exemplo que a maçaneta está mais fria do que a porta. CORRETA.
A sensação de que a maçaneta de metal está mais fria que a porta de madeira ocorre pois a taxa de calor transferido do corpo para o metal é maior do que a do corpo para a madeira. Como o metal é um ótimo condutor de calor, ele "rouba" a energia térmica da mão mais rapidamente que a madeira, sendo que esta atua mais como um isolante térmico. Alternativa correta.
d) A energia potencial gravitacional depende da escolha do referencial adotado. INCORRETA.
A energia potencial gravitacional é uma grandeza escalar, que é definida a partir de um referencial adotado. Alternativa correta.
e) O módulo do empuxo exercido por um liquido sobre um corpo totalmente submerso nesse liquido é sempre igual ao módulo do peso do corpo. INCORRETA.
O módulo do empuxo exercido por um líquido é igual ao módulo do peso do volume de líquido deslocado, que pode ser igual ou não ao módulo do peso do corpo. Alternativa incorreta.
Como há duas alternativas corretas, a questão foi devidamente anulada.
1713) Leia o texto a seguir, completando as lacunas, com os termos adequados.
- A) calor específico, menor e esfriando-se.
- B) capacidade térmica, menor e esfriando-se.
- C) calor específico, maior e aquecendo-se.
- D) capacidade térmica, maior e aquecendo-se.
Questão:
Um veranista, ao visitar a praia de água doce da Lagoa dos Patos, em Arambaré-RS, percebe uma diferença na temperatura da água da lagoa em relação à areia da praia, ou seja, durante o dia, a areia está mais quente do que a água; já à noite, ocorre a inversão, a água fica mais aquecida que a areia. Esse fenômeno ocorre porque a areia possui calor específico menor que da água, sendo a quantidade de energia necessária para aquecer a areia menor e, por isso, seu aquecimento ocorre mais rápido. Durante a noite, a areia também perde energia mais facilmente que a água, esfriando-se mais rapidamente.
Os termos que completam correta e respectivamente as lacunas são:
- A) calor específico, menor e esfriando-se.
Explicação:
A areia tem um calor específico menor que a água, o que significa que ela necessita de menos energia para aumentar sua temperatura. Além disso, a areia também perde calor mais rápido que a água, esfriando-se mais rapidamente. Isso explica por que a areia está mais quente que a água durante o dia e mais fria à noite. A capacidade térmica da areia é menor que a da água, o que faz com que ela se aqueça e esfrie mais rapidamente.
1714) De acordo com o site CLIMATE-DATA.ORG, a temperatura média anual em Camaquã é 18,9 °C, sendo de 24,3 °C a temperatura média do mês de janeiro, o mês mais quente do ano, e de 14,1 °C a temperatura média do mês de junho, média mais baixa de todo o ano.
- A) 5,40
- B) 10,2
- C) 287,25
- D) 297,45
Para encontrar a variação de temperatura entre o mês mais quente e o mais frio em Kelvin, precisamos converter as temperaturas de Celsius para Kelvin.
Primeiramente, convertamos as temperaturas de Celsius para Kelvin:
Temperatura média do mês de janeiro (24,3°C): 24,3°C + 273,15 = 297,45 K
Temperatura média do mês de junho (14,1°C): 14,1°C + 273,15 = 287,25 K
Agora, para encontrar a variação de temperatura, subtrairemos a temperatura do mês de junho da temperatura do mês de janeiro:
Variação de temperatura = 297,45 K - 287,25 K = 10,2 K
Portanto, a alternativa correta é a letra B) 10,2.
Essa resposta é correta porque realizamos a conversão das temperaturas de Celsius para Kelvin e, em seguida, encontramos a variação de temperatura subtraindo a temperatura do mês de junho da temperatura do mês de janeiro.
1715) Um termõmetro registra a temperatura de 932 ºF. Converta esse valor para a escala Celsius e marque a opção correta.
- A) 100
- B) 200
- C) 300
- D) 400
- E) 500
A alternativa correta é letra E) 500
Gabarito: LETRA E.
Para encontrar a relação correta entre duas escalas, é preciso conhecer pelo menos 2 pontos em comum. Assim, podemos desenvolver o seguinte esquema:
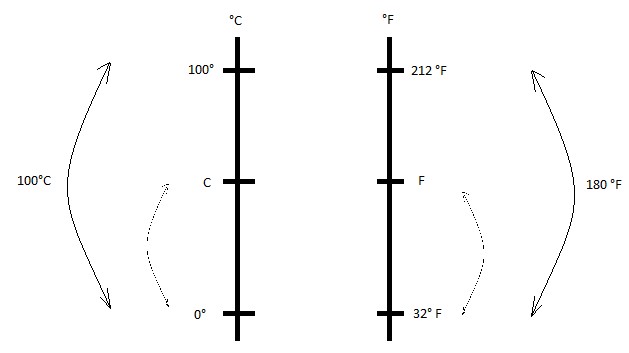
Dessa forma, podemos estabelecer uma relação de proporção entre os segmentos das escalas em °C e ºF. Logo,
dfrac {C - 0} {100 - 0} = dfrac {F-32} {212-32}
dfrac {C} {100} = dfrac {F-32} {180}
C = dfrac {F-32} {1,8}
Substituindo-se o valor do enunciado, temos:
C = dfrac {932-32} {1,8}
C = 500 °C
Portanto, a resposta correta é a alternativa (e).
Questão 1716
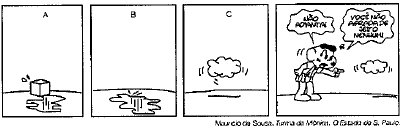
De acordo com os quadrinhos acima, é correto afirmar que as mudanças de estados físicos apresentados na sequência A–> B e B –> C são, respectivamente
- A) fusão e condensação.
- B) sublimação e liquefação.
- C) liquefação e vaporização .
- D) solidificação e condensação.
- E) fusão e vaporização.
A alternativa correta é letra E) fusão e vaporização.
Gabarito: LETRA E.
Na sequência A --> B, é possível verificar que possivelmente trata-se de água passando do estado sólido para o estado líquido, ou seja, trata-se da fusão da água.
Já na sequência B --> C, podemos verificar que a água passa do estado líquido para o gasoso, ou seja, trata-se da vaporização da água.
Portanto, a resposta correta é a alternativa (e).
1717) Considerando um 1 kg de gelo de água e desprezando as perdas de calor para o ambiente e a evaporação da água, assinale qual a opção que fornece o calor, em kilocalorias, necessário para transformar o gelo de água inicialmente á temperatura de – 20 ºC em vapor de água á 100 ºC.
- A) 340
- B) 520
- C) 730
- D) 890
- E) 920
A alternativa correta é letra C) 730
Questão que requer a quantidade de energia para modificar a temperatura da água.
Porém, o candidato(a) deve ficar atento(a) para os calores específicos nos diferentes estados físicos.
Temos a seguinte informação: a massa de 1kg = 1.000g.
Sabemos que uma caloria é a quantidade de energia (calor) necessária para aumentar em 1 ºC a temperatura de um grama de água.
As variações de temperatura exigirão certos valores. E iremos calcular a somatória destes valores.
Temos o gelo em temperatura inicial de -20º C e ele será aquecido até 0ºC, temperatura em que ocorrerá a fusão.
A relação de calor (Q) corresponde a Q = mc ΔT.
Q = calor
m = massa da substância = 1.000g
ΔT = 20
C = 0,5 cal/g·ºC
Substituindo, teremos:
Q = 1.000*0,5*20 = 10.000 calorias.
Pronto, agora o gelo atingiu a temperatura de 0º C e precisa de energia para fundir e se tornar líquido.
Vamos usar o calor latente da água, pois, calor latente da substância é grandeza que determina a quantidade de calor necessária para que 1 g da substância mude o seu estado físico.
Se temos 1.000g de água teremos a necessidade de fornecer 80 cal/g. Logo, QL = L*m.
Assim, temos:
QL = 80*1.000 = 80.000 calorias
Agora a massa líquida precisa atingir a temperatura de 100ºC.
Para isso irá requerer calor, que calcularemos usando a mesma expressão matemática inicial: Q = mc ΔT.
Q = calor
m = massa da substância = 1.000g
ΔT = 100
C = 1,0 cal/g·ºC
Substituindo, teremos:
Q = 1.000*1*100 = 100.000 calorias.
Resta aquecer esta massa para que ela se transforme em vapor.
Se temos 1.000g de água teremos a necessidade de fornecer 540 cal/g. Logo, QL = L*m.
Assim, temos:
QL = 540*1.000 = 540.000 calorias
A somatória das calorias para cada etapa corresponde a 730.000 calorias, ou, 730 kcal.
1718) Colocou-se certa massa de água a 80 ºC em um recipiente de alumínio de massa 420 g que estava à temperatura de 20 ºC. Após certo tempo, a temperatura do conjunto atingiu o equilíbrio em 70 ºC. Considerando que a troca de calor ocorreu apenas entre a água e o recipiente, que não houve perda de calor para o ambiente e que os calores específicos do alumínio e da água sejam, respectivamente, iguais a 9,0 x 102 J/(kg ⋅ ºC) e 4,2 x 103 J/(kg ⋅ ºC), a quantidade de água colocada no recipiente foi
- A) 220 g.
- B) 450 g.
- C) 330 g.
- D) 520 g.
- E) 280 g.
A alternativa correta é letra B) 450 g.
Como o sistema recipiente + líquido está isolado, a quantidade de calor perdida pela água deve ser igual à quantidade de calor recebida pelo recipiente.
Desprezando os sinais, temos que:
| Q_A | = | Q_R |
m_A times c_A times | Delta theta_A | = m_R times c_R times | Delta theta_R
Em que Q, m, c e Delta theta são respectivamente a quantidade de calor, massa, calor específico e variação de temperatura. O subscrito "A" refere-se à água e o subscrito "R" refere-se ao recipiente.
A água tem massa m_A em gramas, calor específico c_A = 4,2 times 10^3~J/(Kg cdot ^circ C) e a temperatura variou de 80oC para 70oC.
O recipiente de alumínio tem massa de m_R = 420 g, calor específico de 9 times 10^2 ~J/(Kg cdot ^circ C)~ e a temperatura variou de 20oC para 70oC.
Substituímos esses valores na fórmula:
m_A times 4,2 times10^3 ~J/(Kg cdot ^circ C)~ times |70-80| ^circ C =
= 420 ~g ~ times 9 times 10^2 ~J/(Kg cdot ^circ C)~ times |70-20| ^circ C
Simplificamos a equação:
m_A times 4,2 times10^3 times |70-80| = 420 times 9 times 10^2 times |70-20| ~g
m_A times 4,2 times10^3 times 10 = 420 times 9 times 10^2 times 50~g
m_A = dfrac{420 times 9 times 100 times 50}{4,2 times 10^3 times 10} ~g
m_A = dfrac{100 times 9 times 100 times 50}{1 times 10^3 times 10} ~g
m_A = dfrac{9 times 5 times 10^5 ~g}{10^4} = 450 ~g
Gabarito: Letra B.
1719) Considere que um fogão forneça um fluxo constante de calor e que esse calor seja inteiramente transferido da chama ao que se deseja aquecer. O calor específico da água é 1,00 cal/(g ⋅ ºC) e o calor específico de determinado óleo é 0,45 cal/(g ⋅ ºC). Para que 1 000 g de água, inicialmente a 20 ºC, atinja a temperatura de 100 ºC, é necessário aquecê-la por cinco minutos sobre a chama desse fogão. Se 200 g desse óleo for aquecido nesse fogão durante um minuto, a temperatura desse óleo será elevada em, aproximadamente,
- A) 120 ºC.
- B) 180 ºC.
- C) 140 ºC.
- D) 160 ºC.
- E) 100 ºC.
A alternativa correta é letra B) 180 ºC.
Gabarito: LETRA B
Calcularemos inicialmente a potência térmica do fogão usando os dados fornecidos para o aquecimento da água:
P = frac{Q}{Delta t}
Q = m.C_p.Delta T
Dados fornecidos
m=1000g
C_P=1,00 cal/(g ⋅ ºC)
Delta T = T - T_0=100-20=80°C
Delta t = 5min = 5 times 60s = 300s
Calculando o calor necessário para aquecer a água até 80°C.
Q = m.C_p.Delta T
Q = 1000.1.80=80000~cal
Calculando a potência do fogão
P = frac{Q}{Delta t}
P = frac{80000}{300}approx 266,7~W
Como a potência do fogão é constante, determinaremos a variação de temperatura causada no óleo para um intervalo de tempo de 1min.
Dados sobre o óleo
C_P = 0,45 cal/(g ⋅ ºC)
m=200g
Delta T=????
Delta t = 1min = 1 times 60s = 60s
Calculando a variação de Temperatura do óleo:
P = frac{Q}{Delta t}
266,7=frac{200.0,45.Delta T}{60}
Delta T = frac{266,7}{1,5}=177,8approx 180°C
Gabarito: LETRA B
1720) (URCA/2019.1) O calor latente de fusão da água é 333 𝑘𝐽/𝑘𝑔. Sabendo que o ponto de fusão da água ocorre aproximadamente a 273 𝐾. Determine a quantidade de calor necessário para derreter 500g de água a 0°𝐶 sabendo que 1 𝑐𝑎𝑙=4,2 𝐽. Marque a opção que melhor fornece esse valor.
- A) 39,6 𝑐𝑎𝑙
- B) 39,6 𝐽
- C) 39,6 𝐾𝐽
- D) 166,5 𝐾𝑐𝑎𝑙
- E) 39,6 𝐾𝑐𝑎𝑙
A alternativa correta é letra E) 39,6 𝐾𝑐𝑎𝑙
ALTERNATIVA CORRETA: LETRA E
Dados da questão:
m=500g = 0,5 Kg
L_{Fusão}=333KJ/Kg
Q = m.L = 0,5 . 333 = 166,5KJ
convertendo 166,5KJ para Kcal, basta dividirmos esse valor por 4,2, que o fator de conversão.
Q = frac{166,5}{4,2}=39,64 cong 39,6Kcal
