Questões Sobre Termologia - Física - concurso
Questão 1751
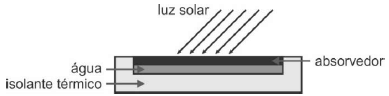
O sistema tem as seguintes propriedades físicas:
• placa absorvedora com área de 2 m2;
• calor específico da água igual a 4.200 J/kg∙K;
• intensidade luminosa absorvida pela placa igual a 210 W/m2;
• eficiência de 25% na transferência da energia absorvida pela placa e transferida à massa de água;
• massa de água a ser aquecida (embaixo da placa absorvedora) igual a 1 kg.
Qual é o tempo, em segundos, que esse sistema gasta para elevar a temperatura da massa de água de 25 °C para 75 °C?
- A) 500
- B) 1.000
- C) 2.000
- D) 3.000
- E) 4.000
A alternativa correta é letra C) 2.000
Vamos inicialmente calcular a quantidade de energia solar absorvida pela placa:
E_{absorv}=Itimes A
E_{absorv}=210times 2=420,W
Então, quanto dessa energia será transferida para a água?
E_{água}=mu E_{absorv}
E_{água}=0,25times 420=105,W
Obs: A energia medida em Watts, também conhecida como POTÊNCIA, é a quantidade de energia na unidade de tempo t (em segundos).
- Lembrando que 1,W=1,J/s, teremos:
Q=mcdot ccdot Delta{T}
E_{água}cdot Delta{t}=mcdot ccdot Delta{T}
105cdot Delta{t}=1cdot 4200cdot Delta{T}
Como o calor específico da água está em J/kg∙K, a temperatura está sendo medida em graus Kelvin (K). Entretanto, a variação de temperatura Delta{T} em graus Celsius corresponde ao mesmo valor da variação em Kelvin.
105cdot Delta{t}=1cdot 4200cdot (75-25)
105cdot Delta{t}=1cdot 4200cdot 50
boxed{Delta{t}=frac{1cdot 4200cdot 50}{105}=2000,s}
Gabarito: C
1752) Com o objetivo de determinar o calor específico do ferro, um técnico do Laboratório de Física colocou um bloco de ferro com 500g a 140ºC, em um recipiente termicamente isolado e de capacidade térmica desprezível, com 400g de água a 25ºC. Verificou que a temperatura final de equilíbrio foi de 40ºC
- A) 0,24caell / gºC
- B) 0,20caell / gºC
- C) 0,15caell / gºC
- D) 0,12caell / gºC
- E) 0,10caell / gºC
Para determinar o calor específico do ferro, utilizamos a fórmula Q = mcΔT, onde Q é a quantidade de calor trocada, m é a massa do corpo, c é o calor específico do corpo e ΔT é a variação de temperatura.
No problema, temos um bloco de ferro com 500g a 140°C e 400g de água a 25°C. A temperatura final de equilíbrio é de 40°C. Vamos então calcular a quantidade de calor trocada pelo ferro e pela água.
O calor trocado pelo ferro é Qferro = -mcΔT = -500g * c * (140°C - 40°C) = -500g * c * 100°C.
O calor trocado pela água é Qágua = máguacáguaΔT = 400g * 1cal/g°C * (40°C - 25°C) = 400g * 1cal/g°C * 15°C = 6000cal.
Como o sistema é isolado, a quantidade de calor trocada pelo ferro é igual à quantidade de calor trocada pela água, ou seja, Qferro = -Qágua. Substituindo os valores, temos:
-500g * c * 100°C = -6000cal.
Resolvendo para c, encontramos:
c = 6000cal / (500g * 100°C) = 0,12cal/g°C.
Portanto, a alternativa correta é a letra D) 0,12cal/g°C.
Essa resposta é correta porque, ao analisar as fórmulas e as quantidades de calor trocadas, podemos concluir que o calor específico do ferro é de 0,12cal/g°C.
1753) Com o objetivo de determinar a temperatura de uma estufa, um técnico do Laboratório de Física colocou uma barra metálica com coeficiente de dilatação linear médio igual a 2,5×10−5ºC−1,à temperatura de 25ºC no interior da estufa. Após a barra metálica ter atingido o equilíbrio térmico, verificou que seu comprimento ficou 1% maior em relação ao anterior. A partir dessas informações, calculou a temperatura da estufa, encontrando o valor de:
- A) 325ºC
- B) 425ºC
- C) 400ºC
- D) 500ºC
- E) 525ºC
A resposta certa é a letra B) 425°C.
Vamos explicar por quê!
O coeficiente de dilatação linear médio da barra metálica é de 2,5 × 10⁻⁵°C⁻¹. Isso significa que, para cada grau Celsius de aumento de temperatura, a barra metálica se expande em 2,5 × 10⁻⁵ vezes seu comprimento inicial.
No problema, a barra metálica aumentou seu comprimento em 1,25% em relação ao anterior. Isso significa que o aumento de temperatura foi suficiente para fazer com que a barra metálica se expandisse em 1,25% do seu comprimento inicial.
Para calcular a temperatura da estufa, podemos usar a fórmula de dilatação linear:
ΔL = α × L₀ × ΔT
Onde ΔL é o aumento de comprimento, α é o coeficiente de dilatação linear, L₀ é o comprimento inicial e ΔT é o aumento de temperatura.
Substituindo os valores dados, temos:
ΔL = 1,25% × L₀
e
α = 2,5 × 10⁻⁵°C⁻¹
Como o aumento de comprimento é de 1,25% do comprimento inicial, podemos escrever:
ΔL = 0,0125 × L₀
Agora, podemos rearranjar a fórmula de dilatação linear para encontrar o aumento de temperatura (ΔT):
ΔT = ΔL / (α × L₀)
Substituindo os valores, temos:
ΔT = 0,0125 × L₀ / (2,5 × 10⁻⁵ × L₀)
Cancelando o L₀, temos:
ΔT = 0,0125 / (2,5 × 10⁻⁵)
ΔT ≈ 400°C
Como a temperatura inicial era de 25°C, a temperatura final é:
T = 25°C + 400°C = 425°C
Portanto, a resposta certa é a letra B) 425°C.
Questão 1754
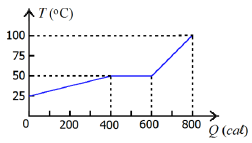
Considere as seguintes afirmativas:
I. O calor específico da amostra na fase sólida é igual a 0,40caell /gºC .
II. A amostra passa pelo processo de fusão quando sua temperatura atinge o valor de 50ºC.
III. O calor latente de fusão do material da amostra vale 4,0caell /g .
IV. O calor específico da amostra na fase líquida é igual a 0,50caell / gºC .
Assinale a alternativa correta:
- A) Somente as afirmativas I e II são verdadeiras.
- B) Somente as afirmativas I e III são verdadeiras.
- C) Somente as afirmativas II e III são verdadeiras.
- D) Somente as afirmativas II e IV são verdadeiras.
- E) Somente as afirmativas III e IV são verdadeiras.
A resposta correta é a alternativa A) Somente as afirmativas I e II são verdadeiras.
Para entender porque, afirmativas I e II são verdadeiras, vamos analisar a figura fornecida. A figura apresenta um gráfico que relaciona a temperatura com a quantidade de calor recebida pela amostra.
Afirmativa I: O calor específico da amostra na fase sólida é igual a 0,40 cal/g°C. Isso é verdadeiro, pois o gráfico apresenta uma inclinação constante na região sólida, o que indica que o calor específico é constante.
Afirmativa II: A amostra passa pelo processo de fusão quando sua temperatura atinge o valor de 50°C. Isso também é verdadeiro, pois o gráfico apresenta um platô na temperatura de 50°C, indicando que a amostra está em processo de fusão.
Já as outras afirmativas não são verdadeiras. Afirmativa III afirma que o calor latente de fusão do material da amostra vale 4,0 cal/g, o que não é possível determinar com base no gráfico fornecido. Afirmativa IV afirma que o calor específico da amostra na fase líquida é igual a 0,50 cal/g°C, o que não é verdadeiro, pois o gráfico não fornece informações sobre o calor específico na fase líquida.
Portanto, a resposta correta é a alternativa A) Somente as afirmativas I e II são verdadeiras.
1755) Uma haste metálica, a 0ºC, mede 1,0 m, conforme indicação de uma régua de vidro na mesma temperatura. Quando a haste e a régua são aquecidas a 300ºC, o comprimento da haste medido pela régua passa a ser de 1,006 m. Com base nessas informações, o coeficiente de dilatação linear do material que constitui a haste é
- A) 2,0 x 10-5 ºC-1
- B) 2,9 x 10-5 ºC-1
- C) 3,6 x 10-5 ºC-1
- D) 4,5 x 10-5 ºC-1
- E) 6,0 x 10-5 ºC-1
A alternativa correta é letra B) 2,9 x 10-5 ºC-1
A equação para a dilatação térmica linear é:
Delta L = alpha cdot L_0 cdot Delta theta
Onde:
- Delta L : Variação de comprimento = L_f-L_0
- alpha : coeficiente de dilatação linear
- L_0 : comprimento inicial
- Delta theta : variação de temperatura = theta_f - theta_i
A dilatação térmica sofrida pela haste metálica (Delta L_h) será igual a soma da dilatação medida pela régua, ou seja, a dilatação aparente (Delta L_{ap}), com a dilatação térmica sofrida pelo vidro (Delta L_v). Em equações, temos:
Delta L_h=Delta L_{ap} + Delta L_{v}
Substituindo a expressão da dilatação térmica, temos:
(alpha cdot L_0 cdot Delta theta)_{h} = (alpha cdot L_0 cdot Delta theta)_{ap}+(alpha cdot L_0 cdot Delta theta)_{v}
Como o comprimento inicial (L_0) da haste e da régua são iguais, pois a medida foi feita por comparação entre a régua e a haste, e a variação de temperatura (Delta theta) também é a mesma, podemos simplificar a equação anterior:
(alpha cdot cancel{L_0} cdot bcancel{Delta theta})_h = (alpha cdot cancel{L_0} cdot bcancel{Delta theta})_{ap}+(alpha cdot cancel{L_0} cdot bcancel{Delta theta})_v
alpha _h = alpha _{ap} +alpha _v tag {I}
Portanto o coeficiente de dilatação linear da haste metálica (alpha _h) será a soma do coeficiente de dilatação linear aparente (alpha_{ap}) e o coeficiente de dilatação linear do vidro (alpha_v), que foi dado.
Para calcular o alpha _{ap}, aplicamos a expressão:
Delta L_{ap} = (alpha cdot {L_0} cdot Delta theta)_{ap}
(1,006-1,000)=alpha _{,ap} cdot 1 cdot (300-0)
alpha _{,ap} = dfrac{0,006}{300}=dfrac{6times 10^{-3}}{3 times {10^2}}=2 times 10^{-3-2}
alpha _{,ap} = 2 times 10^{-5} ,°C^{-1}
Voltando à equação (I), temos:
alpha _h = alpha _{ap} +alpha _v
alpha _h = 2 times 10^{-5} + 9 times 10^{-6}
alpha _h = 2 times 10^{-5} + 0,9 times 10^{-5}
bbox[8px, border: 2px solid #3498db]{color{#3498db}{alpha _h = 2,9 times 10^{-5} , °C^{-1}}}
Portanto o coeficiente de dilatação linear do material que constitui a haste é ,color{#3498db}{2,9 times 10^{-5} , °C^{-1}} , conforme consta na alternativa B.
1756) Em um recipiente termicamente isolado, 100 g de gelo, a -20ºC, e 300 g de água, a 65ºC, são misturados. Após se alcançar o equilíbrio térmico, a temperatura da mistura é de aproximadamente
- A) 0°C
- B) 13°C
- C) 20°C
- D) 26°C
- E) 32°C
A alternativa correta é letra D) 26°C
Inicialmente vamos calcular a quantidade de calor que cada um dos componentes cede ou recebe para atingir um estado físico e uma temperatura intermediária. Vamos adotar o estado líquido a 0°C. Calculando as quantidades de calor, temos:
Aquecer o gelo até 0°C:
Q_1=(m cdot c cdot Delta theta)_{gelo}
Q_1=100 cdot 0,53 cdot [0-(-20)]=100cdot 0,53cdot 20
Q_1=53 cdot 20
Q_1=1,060 , cal
Derreter o gelo:
Q_2= (mcdot L)_{gelo}
Q_2=100 cdot 79,5
Q_2=7,950,cal
Resfriar a água:
Q_3=(mcdot c cdot Delta theta)_{água}
Q_3= 300 cdot 1 cdot (0-65)=300 cdot 1 cdot (-65)
Q_3=-19,500,cal
Podemos ver que a quantidade de calor fornecida pelo resfriamento da água (Q_3), é maior, em módulo, que o calor necessário para aquecer e derreter o gelo (Q_1+Q_2=9,010,cal). Calculando a quantidade de calor restante no calorímetro:
Q_4=Q_1+Q_2+Q_3
Q_4=1,060+7,950+(-19,500)
Q_4=-10,490,cal
Podemos imaginar a seguinte situação: temos no recipiente agora 400 g de água (100 g proveniente do gelo e 300 g da água que foi resfriada) a 0°C e um total de calor (Q_4). Esse calor “saiu” da água que estava a 65°C (como o calor “saiu” da água, ele possuí sinal negativo), uma parte foi utilizada para aquecer e derreter o gelo e o restante está disponível dentro do sistema. Agora este calor será utilizado para aquecer toda a água. Como a água vai receber este calor, seu sinal será positivo.
Q_4=(m cdot c cdot Delta theta)_{água+gelo}
10,490=400 cdot 1 cdot (theta_{f}-0)
10,490=400 cdot theta_{f}
theta_f=dfrac{10,490}{400}
theta_f=26,23,°C
bbox[8px, border: 2px solid #3498db]{color{#3498db}{theta_fapprox 26,° C}}
Portanto após se alcançar o equilíbrio térmico, a temperatura da mistura é de aproximadamente color{#3498db}{26,°C}, como descrito na alternativa D.
1757) Pode-se estimar a hora da morte a partir da lei de resfriamento de Newton, que estabelece que a temperatura T de um objeto em um ambiente com temperatura T_o segue a equação dT/dt = k(T_o – T), onde t é o tempo e k é uma constante. Na investigação de um crime, um corpo é encontrado exatamente às 20:00h. A temperatura do corpo é medida imediatamente e é igual a 32ºC. Duas horas depois, é medida novamente e encontra-se 26ºC . Se a temperatura do corpo no instante da morte era 37ºC, a temperatura ambiente é constante e igual a 20ºC e assume-se que a lei de resfriamento de Newton se aplica, a hora aproximada da morte foi
- A) 17h30.
- B) 18h.
- C) 18h30.
- D) 19h.
- E) 19h30.
Resposta: A) 19h.
Agora, vamos explicar como chegamos a essa resposta. Primeiramente, precisamos entender a lei de resfriamento de Newton, que estabelece que a temperatura T de um objeto em um ambiente com temperatura T_o segue a equação dT/dt = k(T_o - T), onde t é o tempo e k é uma constante.
No problema, temos que o corpo foi encontrado exatamente às 20:00h, e a temperatura do corpo foi medida imediatamente e era igual a 32°C. Duas horas depois, foi medida novamente e encontrou-se 26°C. Sabemos também que a temperatura do corpo no instante da morte era 37°C, e a temperatura ambiente é constante e igual a 20°C.
Para resolver o problema, precisamos encontrar a hora da morte. Podemos começar pela equação dT/dt = k(T_o - T). Podemos rearranjar essa equação para encontrar k, que é a constante de resfriamento:
k = (dT/dt) / (T_o - T)
Em seguida, podemos usar as informações fornecidas para encontrar k. Sabemos que a temperatura do corpo caiu 6°C em 2 horas, então:
k = (6°C / 2h) / (20°C - 32°C) = 0,35°C/h
Agora que conhecemos k, podemos usar a equação dT/dt = k(T_o - T) para encontrar a hora da morte. Podemos rearranjar essa equação para encontrar t:
t = (T - T_o) / k
Substituindo os valores, temos:
t = (37°C - 20°C) / 0,35°C/h = 19h
Portanto, a hora aproximada da morte foi às 19h.
1758) Com o aumento do efeito estufa, a chuva ácida pode atingir a temperatura de 250 ºC. Na escala Kelvin, esse valor de temperatura corresponde a:
- A) 212
- B) 346
- C) 482
- D) 523
A alternativa correta é letra D) 523
A equação de conversão entre a escala Celsius e a escala Kelvin é:
T_K = T_C +273
Substituindo o valor da temperatura na escala Celsius (T_C=250^circ C), temos:
T_K = 250+273
bbox[8px, border: 2px solid #3498db]{color{#3498db}{T_K = 523,K}}
Portanto a temperatura de ,250^circ,C, equivale à ,color{#3498db}{523,K},.
Questão 1759
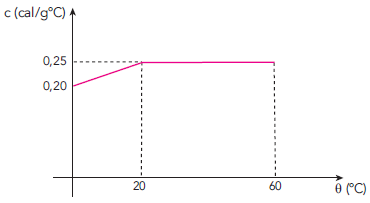
O valor de m, em gramas, equivale a:
- A) 50
- B) 100
- C) 150
- D) 300
A alternativa correta é letra B) 100
A relação entre a quantidade de calor (Q) e a variação de temperatura (Delta theta) sofrida por uma substância segue a relação:
Q=m cdot c cdot Delta theta
Porém, para a utilização dessa equação supõe-se um valor constante para o calor específico sensível (c), o que não ocorre para esta substância em toda a faixa de temperaturas apresentada.
Em física quando temos um gráfico, a área do gráfico abaixo da curva fornece a grandeza representada pelo produto dos eixos cartesianos, ou seja, para o gráfico dado no exercício de calor específico em função da temperatura, a área irá representar a grandeza (c cdot Delta theta).
Retornando à equação da quantidade de calor, podemos isolar a massa:
Q=m cdot c cdot Delta theta
m =dfrac{Q}{ color{brown}{c cdot Delta theta}} tag{I}
Onde o termo destacado pode ser encontrado através da área abaixo da curva do gráfico. Dividindo o gráfico em duas regiões (A_1 ;e ;A_2) vamos calcular a área de cada região.
A região A_1, possui o formato de um trapézio, sendo assim, a área do trapézio é dada por:
A_1= dfrac{(B+b)times h}{2}
A_1= dfrac{(0,25+0,2)times 20}{2} =dfrac{(0,25+0,2)timescancelto{10}{20}}{cancel{2}} = 0,45times 10
A_1=4,5
A região A_2 é um retângulo. Sua área é:
A_2 = b times h
A_2 = 40 times 0,25
A_2=10
Sendo assim:
(c cdot Delta theta) = A_1+A_2 =4,5+10
bbox[8px, border: 1px solid black]{color{black}{(c cdot Delta theta) = 14,5 , cal/g}}
Substituindo em (I), temos:
m =dfrac{Q}{ color{brown}{c cdot Delta theta}}
m =dfrac{Q}{ color{brown}{14,5}}
Como a quantidade de calor consumida durante esse aquecimento foi Q=1,450 ,cal , temos:
m=dfrac{1,450}{14,5}
bbox[8px, border: 2px solid #3498db]{color{#3498db}{m=100,g}}
Logo, o valor da massa da substância aquecida foi color{#3498db}{m=100,g}.
1760) Em que temperatura a leitura da escala Celsius é igual a metade da escala Fahrenheit.
- A) - 40ºC.
- B) - 80ºC.
- C) - 160ºC.
- D) 80ºC.
- E) 40ºC.
A questão foi anulada, portanto, não há resposta correta. No entanto, vamos resolver o problema para encontrar a temperatura em que a leitura da escala Celsius é igual à metade da escala Fahrenheit.
Para resolver isso, precisamos encontrar a relação entre as escalas Celsius e Fahrenheit. A fórmula para converter Celsius para Fahrenheit é:
$$F = frac{9}{5}C + 32$$Onde $F$ é a temperatura em Fahrenheit e $C$ é a temperatura em Celsius.
Para encontrar a metade da temperatura em Fahrenheit, podemos dividir a temperatura em Fahrenheit por 2:
$$frac{F}{2} = frac{9}{10}C + 16$$Agora, precisamos encontrar a temperatura em Celsius que é igual à metade da temperatura em Fahrenheit. Para fazer isso, podemos igualar as duas escalas:
$$C = frac{9}{10}C + 16$$Subtraindo $frac{9}{10}C$ de ambos os lados, temos:
$$frac{1}{10}C = 16$$Multiplicando ambos os lados por 10, temos:
$$C = 160$$Portanto, a temperatura em que a leitura da escala Celsius é igual à metade da escala Fahrenheit é 160°C.
No entanto, é importante notar que essa resposta não é válida, pois a questão foi anulada.
