Questões Sobre Termologia - Física - concurso
1801) Um forno capaz de fornecer 3000 cal/min é utilizado para derreter metal. Deseja-se utilizar esse forno para derreter uma peça de alumínio de massa m= 300 g cuja temperatura de fusão é 660 ºC. A peça de alumínio é colocada no forno com uma temperatura inicial de 30 ºC. O tempo mínimo necessário para o derretimento completo da peça de alumínio, desprezando quaisquer perdas de energia, será de:
- A) 6 min
- B) 12 min
- C) 22 min
- D) 30 min
- E) 66 min
A alternativa correta é letra C) 22 min
Gabarito: LETRA C.
Para o derretimento completo da peça de alumínio, o forno deve fornecer uma quantidade de calor Q_1 para aquecê-la de 30° a 660°C, e depois uma quantidade de calor Q_2 necessária para fundir a peça.
O calor Q_1 é chamado de calor sensível, e é dado por
Q_1 = m c Delta theta
Logo,
Q_1 = 300 cdot 0,2 cdot left( 660 - 30 right)
Q_1 = 37.800 , cal
O calor Q_2 é chamado de calor latente, e é dado por
Q_2 = m L
Q_2 = 300 cdot 94
Q_2 = 28.200 , cal
Então, temos que
Q_{total} = Q_1 + Q_2
Q_{total} = 37.800 + 28.200
Q_{total} = 66.000 , cal
A potência do forno é dada pela taxa temporal de calor fornecido, ou seja,
P = dfrac { Q_{total} } { Delta t }
Logo,
Delta t = dfrac { Q_{total} } { P }
Delta t = dfrac { 66.000 cancel {cal} } { 3.000 cancel {cal} /min }
Delta t = 22 , min
Portanto, a resposta correta é a alternativa (c).
Questão 1802
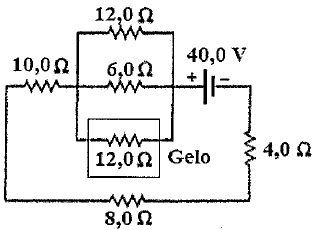
A bateria tem resistência interna desprezível, e o calor latente de fusão para o gelo é de 3,34×105 J/kg. Sendo assim, qual é o valor da taxa (em g/s) em que esse circuito derreterá o gelo?
- A) 0,570x10-5
- B) 0,573x10-4
- C) 0,572x10-3
- D) 0,575x10-2
- E) 0,578x10-1
A alternativa correta é letra D) 0,575x10-2
Gabarito: LETRA D.
Note que o resistor de 12,0 , Omega está inserido em uma associação em paralelo, como os mostra a figura abaixo:
Assim, temos que
dfrac { 1 } { R_{paralelo} } = dfrac { 1 } { 12 } + dfrac { 1 } { 6 } + dfrac { 1 } { 12 }
dfrac { 1 } { R_{paralelo} } = dfrac { 4 } { 12 }
R_{paralelo} = dfrac { 12 } { 4 }
R_{paralelo} = 3, Omega
Assim, a resistência equivalente do circuito é dada por
R_{eq} = R_{paralelo} + 10 + 8 + 4
R_{eq} = 3 + 22
R_{eq} = 25 , Omega
Dessa forma, a corrente que percorre o circuito é dada por:
i = dfrac { U } { R_{eq} }tag 1
i = dfrac { 40 } { 25 }
i = 1,6 , A
Sabendo a corrente, podemos calcular a tensão sobre o resistor de 12 , Omega, que é igual à tensão entre os pontos A e B
U_{AB} = i cdot R_{paralelo}
U_{AB} = 1,6 cdot 3
U_{AB} = 4,8 , V
Sabendo a tensão e a resistência, podemos calcular a potência dissipada pelo resistor de 12 , Omega:
P_{12,Omega} = dfrac { {U_{AB}}^2 } { R_{12,Omega} }
P_{12,Omega} = dfrac { {4,8}^2 } { 12 }
P_{12,Omega} = 1,92 , W
Porém, a potência é a energia consumida por unidade de tempo, ou seja,
P = dfrac { E } { Delta t }
Como essa energia será usada para fundir o gelo, trata-se do calor latente. Logo,
P = dfrac { Q } { Delta t }
P = dfrac { mL } { Delta t }
dfrac { m } { Delta t } = dfrac { P } { L }
dfrac { m } { Delta t } = dfrac { 1,92 cancel J /s } { 3,34 cancel J / kg }
dfrac { m } { Delta t } approx 0,575 , kg/s
dfrac { m } { Delta t } approx 0,575 times 10^3 , g/s
Portanto, a resposta correta é a alternativa (d).
1803) Luiz, um paisagista de jardins, quer utilizar placas quadradas, de lado L, de um material, cujo coeficiente de dilatação linear é alpha, para fazer um caminho para pedestres em um jardim. Sabendo que a temperatura das placas no momento da construção do caminho é 18 ºC e que em dias mais quentes pode atingir a temperatura de 38 ºC, a distância entre as placas para que uma placa não toque na outra devido à dilatação térmica deve ser maior que:
- A) 40 Lalpha
- B) 20 Lalpha
- C) 2L (sqrt {1 + 40alpha - 1}
- D) L (sqrt {1 + 40alpha - 1}
- E) L(1 + 40alpha)
ESTA QUESTÃO FOI ANULADA, NÃO POSSUI ALTERNATIVA CORRETA
Gabarito: ANULADO.
Considere a figura a seguir:
Onde A representa a área da placa de lado L e A' representa a área da placa de lado L', ou seja, após a dilatação. Sabemos que uma placa de área A sofre uma dilatação térmica superficial Delta A devido ao aumento de temperatura Delta T, que é dada por
A' = A + Delta A
A' = A + A beta Delta T
A' = A left( 1 + beta Delta T right)
Onde beta é o coeficiente de dilatação superficial. Porém, sabemos que beta = 2 alpha, onde alpha é o coeficiente de dilatação linear. Assim, a equação acima se torna:
A' = A left( 1 + 2 alpha Delta T right)
Como A' = {L'}^2 e A = L^2, temos que
{L'}^2 = L^2 left( 1 +2 alpha Delta T right)
L' = L sqrt{ 1 + 2 alpha Delta T }
Da figura acima, temos que
dfrac x 2 + L + dfrac x 2 = L'
Logo,
x +L = L'
x = L' - L
Substituindo L', temos que
x = L sqrt{ 1 + 2 alpha Delta T } - L
x = L left( sqrt{ 1 + 2 alpha Delta T } - 1 right)
x = L left( sqrt{ 1 + 2 cdot alpha cdot 20 } - 1 right)
x = L left( sqrt{ 1 + 40 alpha } - 1 right)
O que corresponderia à alternativa (d). Entretanto, a questão foi anulada.
1804) Na ausência de um chuveiro elétrico, um estudante decide, para tomar um banho moro, misturar numa banheira duas panelas com água a 100ºC e oito panelas de mesmo volume com água a 20º. Conclui-se, desprezando as perdas de calor para o ambiente, que a temperatura, em ºC, obtida na água da banheira foi de:
- A) 30
- B) 32
- C) 34
- D) 36
- E) 38
A alternativa correta é letra D) 36
Gabarito: LETRA D.
Quando, em uma mistura, as perdas de calor para o ambiente são desprezadas, o calor recebido por corpos mais frios é cedido por corpos mais quentes, ou seja, a somatória total do calor é nula:
displaystyle sum Q = 0
Como não há mudanças de fase, a questão trata apenas do calor sensível, que é dado por Q = mc Delta theta. Então, para a mistura do enunciado, temos que
Q_1 + Q_2 = 0
m_1 cdot cancel c cdot left( theta_e - theta_{1_{inicial} } right) + m_2 cdot cancel c cdot left( theta_e - theta_{2_{inicial} } right) = 0
m_1 left( theta_e - theta_{1_{inicial} } right) + m_2 left( theta_e - theta_{2_{inicial} } right) = 0
Como são misturadas duas panelas com água a 100ºC e oito panelas de mesmo volume com água a 20º, podemos escrever
2 cancel m left( theta_e - 100 right) + 8 cancel m left( theta_e - 20 right) = 0
2 theta_e - 200 + 8theta_e - 160 = 0
10 theta_e = 360
theta_e = 36, ºC
Portanto, a resposta correta é a alternativa (d).
Questão 1805
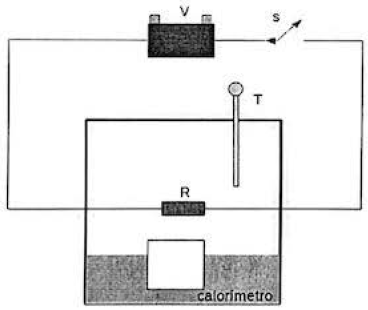
1. colocou-se 100 g de água a 10 ºC e 50 g de gelo com temperatura de – 10 ºC no calorímetro;
2. ligou-se a chave S por 220 s e desligou-se em seguida;
3. esperou-se que o termômetro T indicasse que o sistema (água+ gelo) alcançara o equilíbrio térmico e, então, foi feita a leitura da temperatura interna. Considerando-se que o termômetro e o calorímetro têm capacidade térmica desprezível e toda energia dissipada pelo resistor se converteu em calor, espera se que a temperatura indicada no termômetro T seja de:
(Dados: calor específico do gelo = 0,5 cal/g.ºC; calor específico da água = 1,0 cal/g. ºC; calor latente de fusão do gelo = 80 cal/g; 1 cal = 4 J)
- A) 15 ºC
- B) 20 ºC
- C) 25 ºC
- D) 30 ºC
- E) 35 ºC
A alternativa correta é letra A) 15 ºC
Gabarito: LETRA A.
Primeiramente, vamos calcular a potência dissipada pelo resistor:
P = dfrac { V^2 } { R }
P = dfrac { 10^2 } { 1,0 }
P = 100 , W
Assim, a energia dissipada pelo resistor é dada por
E = P cdot Delta t
E = 100 dfrac J { cancel s }cdot 220 { cancel s }
E = 22000 , J
E = 22000 cancel J cdot dfrac { 1 , cal } { 4 cancel J }
E = 5500 , cal
Toda energia dissipada pelo resistor se converteu em calor, composto por uma quantidade de calor Q_1 que foi responsável por aquecer o gelo, Q_2 para fundi-lo, Q_3 aquecer a massa de água correspondente à massa de gelo inicial até 10°C e Q_4 para aquecer a massa total de água de 10°C até a temperatura final, opu seja,
E = Q_1 + Q_2 + Q_3 + Q_4 tag 1
Como Q_1 é utilizado para aquecer a massa de gelo de -10°C até 0°C, temos
Q_1 = m_{gelo} cdot c_{gelo} cdot left( 0 - left( -10 right) right)
Q_1 = 50 cdot 0,5 cdot 10
Q_1 = 250 , cal
Como Q_2 é utilizado para fundir a massa de gelo, temos
Q_2 = m_{gelo} cdot L_{gelo}
Q_2 = 50 cdot 80
Q_2 = 4000 , cal
Como Q_3 é utilizado para aquecer a massa de água, que é igual à massa de gelo inicial, de 0°C até 10°C, temos
Q_3 = m_{gelo} cdot c_{água} cdot left( 10 - 0 right)
Q_3 = 50 cdot 1,0 cdot 10
Q_3 = 500 , cal
Como Q_4 é utilizado para aquecer a massa total de água de 10°C até a temperatura final theta_f, temos
Q_4 = m_{total} cdot c_{água} cdot left( theta_f - 10 right)
Q_4 = left( 100 + 50 right) cdot 1,0 cdot left( theta_f - 10 right)
Q_4 = 150 cdot left( theta_f - 10 right)
Substituindo em (1), temos que
E = Q_1 + Q_2 + Q_3 + Q_4
5500 = 250 + 4000 + 500 + 150 cdot left( theta_f - 10 right)
5500 = 4750 + 150 cdot left( theta_f - 10 right)
150 cdot left( theta_f - 10 right) = 750
theta_f - 10 = 5
theta_f = 15°C
Portanto, a resposta correta é a alternativa (a).
Questão 1806

Tendo como base as transições de fase representadas (1 a 4), a quantidade de energia absorvida na etapa 2 é igual à quantidade de energia
- A) liberada na etapa 4.
- B) absorvida na etapa 3.
- C) liberada na etapa 3.
- D) absorvida na etapa 1.
- E) liberada na etapa 1.
A alternativa correta é letra E) liberada na etapa 1.
Gabarito: LETRA E.
Observando a figura, podemos verificar que a etapa 1 corresponde à transição de fase do vapor de água para a água líquida, ou seja, a condensação ou liquefação da água. Nesse tipo de transição, o calor é liberado pela água, assim como ocorre nas saunas a vapor: a superfície da pele é aquecida devido à energia liberada pelo vapor de água.
No sentido contrário, a etapa 2 corresponde à transição da água líquida para o vapor de água, ou seja, vaporização. Nesse processo, a energia é absorvida pela água, ao passar do estado líquido para o gasoso.
Como as etapas 1 e 2 são processos inversos, podemos afirmar que a quantidade de energia absorvida na etapa 2 é igual à quantidade de energia liberada na etapa 1.
Portanto, a resposta correta é a alternativa (e).
1807) Em um manual de instruções de uma geladeira, constam as seguintes recomendações:
- A) Reduzir a saída de frio do refrigerador para o ambiente, garantir a transmissão do frio entre os alimentos na prateleira e permitir a troca de calor entre o dissipador de calor e o ambiente.
- B) Reduzir a saída de frio do refrigerador para o ambiente, garantir a convecção do ar interno, garantir o isolamento térmico entre a parte interna e a externa.
- C) Reduzir o fluxo de calor do ambiente para a parte interna do refrigerador, garantir a convecção do ar interno e permitir a troca de calor entre o dissipador e o ambiente.
- D) Reduzir o fluxo de calor do ambiente para a parte interna do refrigerador, garantir a transmissão do frio entre os alimentos na prateleira e permitir a troca de calor entre o dissipador e o ambiente.
- E) Reduzir o fluxo de calor do ambiente para a parte interna do refrigerador, garantir a convecção do ar interno e garantir o isolamento térmico entre as partes interna e externa.
A alternativa correta é letra C) Reduzir o fluxo de calor do ambiente para a parte interna do refrigerador, garantir a convecção do ar interno e permitir a troca de calor entre o dissipador e o ambiente.
Gabarito: LETRA C.
O funcionamento de uma geladeira consiste em retirar calor de seu interior, rejeitando-o para o meio externo. de forma que a parte interna da geladeira fique mais fria.
Assim, o objetivo de manter a porta do refrigerador aberta apenas o tempo necessário é reduzir o fluxo de calor do ambiente para a parte interna do refrigerador.
Note que o que se transfere é o calor e não o frio. Isso porque o frio é uma sensação humana, que ocorre pelo fato do nosso corpo liberar calor para o meio externo. Em baixas temperaturas, sentimos frio quando perdemos calor para o ambiente com muita rapidez. Logo, as alternativas (a) e (b) estão incorretas.
Além disso, é importante não obstruir a circulação do ar com a má distribuição dos alimentos nas prateleiras pois o resfriamento do da parte interna do refrigerador ocorre devido à convecção do ar interno, que nada mais é do que o movimento de um fluido (ar, no caso da geladeira), devido à diferença de temperatura. Logo, a alternativa (d) está incorreta.
Como mencionamos anteriormente, a geladeira retira calor de seu interior para o ambiente externo. Essa rejeição de calor ocorre através do condensador (dissipador serpentinado) atrás da geladeira. Dessa forma, o objetivo de deixar um espaço de, no mínimo, 5 cm entre a parte traseira do produto e a parede é permitir a troca de calor entre o dissipador e o ambiente. Logo, a alternativa (e) está incorreta.
Portanto, a resposta correta é a alternativa (c).
1808) As panelas de pressão reduzem o tempo de cozimento dos alimentos por elevar a temperatura de ebulição da água. Os usuários conhecedores do utensílio normalmente abaixam a intensidade do fogo em panelas de pressão após estas iniciarem a saída dos vapores.
- A) aumento da pressão interna e os riscos de explosão.
- B) dilatação da panela e a desconexão com sua tampa.
- C) perda da qualidade nutritiva do alimento.
- D) deformação da borracha de vedação.
- E) consumo de gás desnecessário.
A alternativa correta é letra E) consumo de gás desnecessário.
Antes de falar da panela de pressão, vamos considerar o cozimento com panela aberta.
COZIMENTO EM ÁGUA COM PANELA ABERTA
Você provavelmente já ouviu falar que, em cozimento com água, a partir do momento que a água está em processo de ebulição, a intensidade do fogo não irá alterar a velocidade de cozimento do alimento.
Essa afirmação parte do pressuposto que o que cozinha o alimento é unicamente a água quente, e não a temperatura da panela. Assim, a partir do momento que inicia a ebulição, a água está a 100oC, e é e essa água quente que irá cozinhar o alimento. Aumentar a intensidade da chama, nesse caso, apenas irá intensificar a ebulição da água, não influenciando na velocidade de cozimento do alimento.
Vamos agora fazer a mesma análise na panela de pressão.
COZIMENTO EM ÁGUA COM PANELA DE PRESSÃO
Na panela de pressão, a medida que a água evapora, o gás não escapa da panela e cria uma pressão sobre o líquido. Com isso, a pressão que o gás exerce sobre a superfície do líquido é superior à pressão atmosférica, provocando aumento do ponto de ebulição da água.
Como consequência, se na panela aberta a água atingiria temperatura de até 100oC, na panela de pressão a água atinge temperaturas superiores a esse valor, como por exemplo, 110 ou 120oC.
Chega um momento em que a velocidade de ebulição se iguala à velocidade de condensação, e a pressão do gás sobre o líquido atinge um valor máximo. Com isso, o ponto de ebulição da água também atinge um valor máximo.
Considere que a temperatura de ebulição chegue, por exemplo, a 120oC. A partir desse momento, podemos abaixar a intensidade da chama, valendo o mesmo raciocínio feito para panela aberta: é a água quente, agora a 120oC, que vai cozinhar o alimento, e uma maior intensidade de chama não resultará em maior temperatura da água.
Não como irá impactar em cozimento mais rápido, reduzimos a intensidade da chama para economizar no consumo de gás.
Gabarito: Letra E.
1809) Mesmo para peixes de aquário, como o peixe arco-íris, a temperatura da água fora da faixa ideal (26 °C a 28 °C), bem como sua variação brusca, pode afetar a saúde do animal. Para manter a temperatura da água dentro do aquário na média desejada, utilizam-se dispositivos de aquecimento com termostato. Por exemplo, para um aquário de 50 L, pode-se utilizar um sistema de aquecimento de 50 W otimizado para suprir sua taxa de resfriamento. Essa taxa pode ser considerada praticamente constante, já que a temperatura externa ao aquário é mantida pelas estufas. Utilize para a água o calor específico 4,0 kJ kg−1 K−1 e a densidade 1 kg L−1.
- A) 4,0 °C
- B) 3,6 °C
- C) 0,9 °C
- D) 0,6 °C
- E) 0,3 °C
A alternativa correta é letra C) 0,9 °C
Primeiramente vamos considerar o sistema de aquecimento ligado, e calcular a energia fornecida ao aquário durante 1 hora, intervalo de tempo correspondente a 3.600 segundos.
A potência do sistema é de P = 50 W. Logo, a energia em forma de calor fornecida ao aquário é dada pela potência multiplicada pelo intervalo de tempo:
Q = P times Delta t
Q = 50 times 3.600~~ J
Caso não perdesse calor e apenas recebesse essa energia do sistema de aquecimento, a temperatura do aquário aumentaria constantemente. Mas como não há aumento da temperatura, concluímos que existe perda de calor para o ambiente com a mesma potência com que recebe, para que assim sua temperatura se mantenha constante.
Conclusão: sabendo que há recebimento de Q = 50 times 3.600~~ J a cada hora e sabendo que a temperatura não muda, concluímos que o aquário perde Q = 50 times 3.600~~ J para o ambiente a cada hora.
Ao interromper o fornecimento de energia, haverá apenas a troca de calor com o ambiente externo mais frio, com o aquário perdendo quantidade de calor Q = 50 times 3.600~~ J a cada hora. Essa perda resultará em redução de temperatura seguindo esta relação:
Q = m c Delta T
Em que Q é a quantidade de calor perdida, m é a massa da água, c é o calor específico da água e Delta T é a variação de temperatura em Kelvin.
O calor específico da água é de dfrac{4.000 ~J}{Kg.K}.
A massa da água pode ser obtida multiplicando sua densidade com o seu volume:
m = dfrac{1 ~kg}{l} times 50 l = 50 kg
Substituímos as medidas na equação Q = m c Delta T:
50 times 3.600 = 50 times 4.000 Delta T
to Delta T = 0,9 ~K
Lembrando que a variação de temperatura em Kelvin tem o mesmo valor da variação de temperatura em graus Celsius. Logo, temos que:
Delta T = 0,9^circ C
Gabarito: Letra C.
1810) Um fabricante de termômetros orienta em seu manual de instruções que o instrumento deve ficar três minutos em contato com o corpo para aferir a temperatura. Esses termômetros são feitos com o bulbo preenchido com mercúrio conectado a um tubo capilar de vidro.
- A) o termômetro e o corpo tenham a mesma energia interna.
- B) a temperatura do corpo passe para o termômetro.
- C) o equilíbrio térmico entre os corpos seja atingido.
- D) a quantidade de calor dos corpos seja a mesma.
- E) o calor do termômetro passe para o corpo.
A resposta correta é a letra C) o equilíbrio térmico entre os corpos seja atingido.
Para entender por que essa é a resposta certa,, temos que analisar o que está acontecendo no procedimento descrito. O fabricante de termômetros orienta que o instrumento deve ficar em contato com o corpo por três minutos para aferir a temperatura. Isso é necessário porque, de acordo com a termodinâmica, é preciso que o termômetro e o corpo estejam em equilíbrio térmico.
O equilíbrio térmico ocorre quando dois corpos ou sistemas estão à mesma temperatura, ou seja, quando não há mais transferência de calor entre eles. Nesse caso, o termômetro e o corpo devem estar à mesma temperatura para que a temperatura do corpo seja medida com precisão.
Se o termômetro não estiver em equilíbrio térmico com o corpo, a temperatura medida não será precisa. Por exemplo, se o termômetro estiver mais quente ou mais frio que o corpo, a temperatura medida será influenciada por essa diferença de temperatura.
Portanto, é necessário que o termômetro e o corpo estejam em contato por um tempo suficiente para que o equilíbrio térmico seja atingido. Somente assim a temperatura medida pelo termômetro será precisa.
As outras alternativas não são corretas porque não descrevem o processo necessário para aferir a temperatura com precisão. A alternativa A) diz que o termômetro e o corpo devem ter a mesma energia interna, o que não é uma condição necessária para a medição de temperatura. A alternativa B) diz que a temperatura do corpo passa para o termômetro, o que não é verdade, pois a temperatura medida é a do corpo, não a do termômetro. A alternativa D) diz que a quantidade de calor dos corpos seja a mesma, o que não é uma condição necessária para a medição de temperatura. A alternativa E) diz que o calor do termômetro passa para o corpo, o que não é verdade, pois o termômetro não transfere calor para o corpo.
