Questões Sobre Termologia - Física - concurso
1881) Em um dia frio de inverno em uma cidade na região Sul do Brasil, a temperatura exterior a uma residência é de 8º C. Com base nessa informação, responda a questão.
- A) 3,4 cal
- B) 3,9 cal
- C) 18,0 cal
- D) 34,0 cal
- E) 39,0 cal
A alternativa correta é letra A) 3,4 cal
O calor sempre flui da maior para a menor temperatura. Sendo assim, ocorrerá um fluxo de calor Phi de dentro da sala para o exterior da casa.
Então, para que a temperatura no interior da sala permaneça constante em 25 ºC ao longo do tempo, um determinada fonte de calor deverá produzir calor na mesma proporção do fluxo de calor que sai da sala. Esse fluxo é dado por:
Phi=kfrac{ADelta{T}}{d}
Onde k é a constante de condutividade térmica, A é a área do vidro da janela, Delta{T} é a diferença de temperatura entre os ambientes interno e externo e d é a espessura do vidro. Logo:
Phi=2times10^{-3}frac{100times(25-8)}{1}
Phi=2times10^{-3}times100times17
boxed{Phi=3,4,cal/s}
Gabarito: A
1882) Em um dia frio de inverno em uma cidade na região Sul do Brasil, a temperatura exterior a uma residência é de 8º C. Com base nessa informação, responda a questão.
- A) 14ºC
- B) 17ºC
- C) 19ºC
- D) 22ºC
- E) 25ºC
A alternativa correta é letra D) 22ºC
A potência é definida com a taxa de energia dissipada na unidade de tempo. Essa taxa de energia dissipada será a energia absorvida pela água no contato com a resistência do chuveiro. Logo:
Pot=frac{Delta{Q}}{Delta{t}}=14cdot10^{3}=4timesfrac{mcDelta{phi}}{Delta{t}}
Onde Delta{phi} é a variação de temperatura e Delta{t} é o intervalo de tempo de 60s da vazão da água.
14cdot10^{3}=4timesfrac{15cdot10^{3}cdot1(phi_{final}-phi_{inicial})}{60}
14cdot10^{3}=4timesfrac{15cdot10^{3}cdot1(phi_{final}-8)}{60}
14=phi_{final}-8
boxed{phi_{final}=22,^oC}
Gabarito: D
Questão 1883
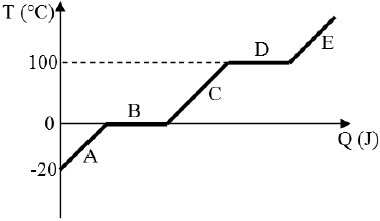
Nas alternativas a seguir, as regiões A, B, C, D e E são representadas por pontos ou por frações de uma reta paralela ao eixo horizontal. Assinale a alternativa que representa corretamente essas 5 regiões no respectivo diagrama de fase da amostra de água pura anteriormente citada.
- A)
- B)
- C)
- D)
A alternativa correta é letra C)
Gabarito: LETRA C.
Observando o gráfico do enunciado, é possível verificar que as regiões A, C e E representam as regiões de aumento de temperatura em resposta ao calor aplicado à amostra de água pura. Por outro lado, as regiões B e D representam patamares de temperatura, nas quais a amostra de água está passando por uma mudança de fase, que são o ponto de fusão (de sólido para líquido) e o ponto de ebulição (de líquido para vapor), respectivamente.
Assim, podemos indicar o estado físico da amostra no gráfico da seguinte maneira:
Para representar as mudanças de estado físico da água em diferentes condições de pressão e temperatura, é comum utilizar um diagrama de fases. A figura a seguir nos mostra um exemplo simplificado do diagrama de fases da água:
Note que durante a mudança de estado físico, a fusão e a vaporização mostradas nas regiões B e D, a temperatura da amostra permanece constante. Isso significa que a pressão é mantida constante, pois a adição de calor está sendo usada exclusivamente para romper as ligações intermoleculares e permitir a transição de fase, sem aumentar a temperatura da substância.
Logo, o aquecimento da amostra de água pura é representado no diagrama de fase da água por uma linha horizontal, já que a temperatura aumenta enquanto a pressão é constante. Além disso, essa linha deve passar por todos os pontos que representamos na figura anterior, como nos mostra a figura a seguir:
Portanto, a resposta correta é a alternativa (c).
1884) A quantidade de quilocalorias de um alimento é determinado em um calorímetro onde uma amostra do alimento é queimada e o calor transferido é medido. No caso de uma amostra de 5 g de um alimento, o calor, por grama da amostra, transferido à 0,5 kg de água pura (1 cal/gºC) colocada dentro desse calorímetro e a 0,1 kg de alumínio (0,2 cal/gºC) que compõe a parte interna desse calorímetro será, em kcal/g, igual a .
- A) 3,72
- B) 4,72
- C) 5,72
- D) 6,72
A alternativa correta é letra C) 5,72
Gabarito: LETRA C.
Aplicando o princípio da conservação da energia, o calor cedido pela queima da amostra é igual ao calor absorvido pela água e pelo alumínio do calorímetro:
Q_{amostra} = Q_{água} + Q_{alumínio} tag 1
Lembrando que o calor Q transferido por uma massa m de uma substância de calor específico c ao sofrer uma variação de temperatura Delta T é dado por
Q = mcDelta T
A equação (1) se torna:
Q_{amostra} = m_{água} cdot c_{água} cdot Delta T_{água} + m_{alumínio} cdot c_{alumínio} cdot Delta T_{alumínio}
Substituindo os valores do enunciado, temos:
Q_{amostra} = 500 cancel g cdot 1,0 dfrac { cal } { cancel g cancel {°C} } cdot 55 cancel {°C} + 100 cancel g cdot 0,2 dfrac { cal } { cancel g cancel {°C} } cdot 55 cancel {°C}
Q_{amostra} = 27500 + 1100
Q_{amostra} = 28600 , cal
Q_{amostra} = 28,6 , kcal
Dividindo o calor pela massa da amostra, temos:
dfrac { Q_{amostra} } m = dfrac { 28,6 , kcal } { 5 , g }
dfrac { Q_{amostra} } m = 5,72 , kcal/g
Portanto, a resposta correta é a alternativa (c).
1885) Os satélites artificiais em órbita da Terra são expostos a ciclos severos de temperatura, pois durante metade da órbita recebem os raios solares intensos e na outra metade não recebem a radiação solar. Portanto, os satélites estão a uma temperatura muito alta na primeira metade da órbita e muito baixa na segunda metade.
- A) -130
- B) 180
- C) 194
- D) 324
A alternativa correta é letra D) 324
Gabarito: LETRA D.
De acordo com o enunciado, a variação de temperatura do teste em graus Celsius é dada por:
Delta °C = 90 - left( -90 right)
Delta °C = 90 + 90
Delta °C = 180°C
Para encontrar uma relação entre duas escalas, é preciso conhecer pelo menos 2 pontos em comum entre elas. Sabemos que a fusão do gelo ocorre em 0°C, o que equivale a 32°F, e a vaporização da água ocorre em 100°C, correspondente a 212°F. Assim, podemos estabelecer uma relação entre as duas escalas como nos mostra a figura a seguir:
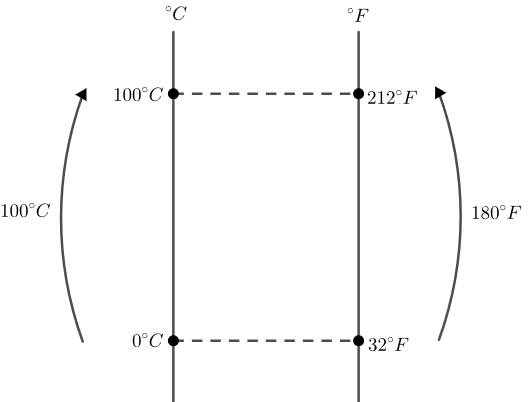
Utilizando a relação de proporção acima, podemos calcular a variação de 180°C na escala Fahrenheit:
begin{array} {cc|cc}°C && °F \ hline 100 && 180 \ 180 && x end{array}
Logo,
100 cdot x = 180 cdot 180
x = dfrac {32400}{100}
x = 324°C
Portanto, a resposta correta é a alternativa (d).
Questão 1886
Na faixa de graus Celsius a escala vai de 5 oC a 60 oC. Esse mesmo intervalo em graus Fahrenheit representa uma faixa de trabalho de oF.
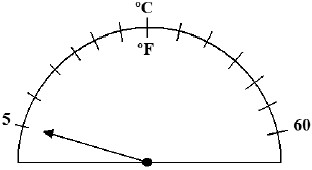
- A) 41
- B) 43
- C) 99
- D) 140
A alternativa correta é letra C) 99
Gabarito: LETRA C.
De acordo com o enunciado, a variação de temperatura do teste em graus Celsius é dada por:
Delta C = 60 - 5
Delta C = 55°C
Para encontrar uma relação entre duas escalas, é preciso conhecer pelo menos 2 pontos em comum entre elas. Sabemos que a fusão do gelo ocorre em 0°C, o que equivale a 32°F, e a vaporização da água ocorre em 100°C, correspondente a 212°F. Assim, podemos estabelecer uma relação entre as duas escalas como nos mostra a figura a seguir:
Observando a figura acima, podemos verificar que uma variação de 100°C corresponde a uma variação de 180°F. Assim, utilizando a relação de proporção acima, podemos calcular a variação de 55°C na escala Fahrenheit da seguinte maneira:
begin{array} {cc|cc}°C && °F \ hline 100 && 180 \ 55 && x end{array}
Logo,
100 cdot x = 55 cdot 180
x = 99°F
Portanto, a resposta correta é a alternativa (c).
1887) Duas amostras “A” e “B” de água no estado líquido de mesma massa (m) e mesmo calor específico (c) possuem temperatura iniciais diferentes TIA e TIB, sendo TIA maior que TIB. A mistura obtida com as duas amostras, após algum tempo, atinge a temperatura final TF.
- A) mc begin {pmatrix} frac {T_{IA} , + , T_{IB}} {2} end {pmatrix}
- B) mc begin {pmatrix} frac {T_{IB} , - , T_{IA}} {2} end {pmatrix}
- C) mc begin {pmatrix} frac {T_{IA} , - , T_{IB}} {2} end {pmatrix}
- D) mc begin {pmatrix} frac {T_{IB} , - , 2T_{IA}} {2} end {pmatrix}
A alternativa correta é letra B) mc begin {pmatrix} frac {T_{IB} , - , T_{IA}} {2} end {pmatrix}
Gabarito: LETRA B.
Lembrando que o calor é dado por:
Q = mcDelta T
Onde m é a massa, c é o calor específico da água e Delta T é a variação de temperatura, a quantidade de calor que a amostra "A" troca é dada por:
Q_A = mc left( T_F - T_{IA} right) tag 1
Analogamente, a quantidade de calor que a amostra "B" troca é dada por
Q_B= mc left( T_F - T_{IB} right) tag 1
Considerando que não há perdas de calor para o ambiente externo, ou seja, se o sistema estivesse completamente isolado, a soma das quantidades de calor que as amostras "A" e "B" trocam é zero. Assim, podemos escrever:
Q_A + Q_B = 0
Logo,
Q_A = - Q_B
Ou seja, a quantidade de calor que uma amostra cede é igual a quantidade de calor que a outra absorve. Assim, temos:
cancel {mc} left( T_F - T_{IA} right) = -cancel {mc} left( T_F - T_{IB} right)
T_F - T_{IA} = -left( T_F - T_{IB} right)
T_F - T_{IA} = -T_F + T_{IB}
2 T_F = T_{IA} + T_{IB}
T_F = dfrac { T_{IA} + T_{IB} } 2
Substituindo T_F na equação (1), temos:
Q_A = mc left[ left( dfrac { T_{IA} + T_{IB} } 2 - T_{IA} right) right]
Q_A = mc left( dfrac { T_{IA} + T_{IB} - 2 T_{IA} } 2 right)
Q_A = mc left( dfrac { T_{IB} - T_{IA} } 2 right)
Note que, como T_{IA} gt T_{IB}, temos que Q_A lt 0. Ou seja, a amostra "A" cede uma quantidade de calor Q_A.
Portanto, a resposta correta é a alternativa (b).
1888) Um engenheiro recebe a tarefa de elaborar um anteprojeto para estabelecer alguns parâmetros de desempenho referentes a uma usina termelétrica a carvão que será empregada em situações emergenciais. Esta usina trabalhará segundo um ciclo termodinâmico e, em seu estudo, o engenheiro estabelece as afirmativas abaixo:
- A) I, apenas.
- B) II, apenas.
- C) I e III, apenas.
- D) I e II, apenas.
- E) I, II e III.
A alternativa correta é letra E) I, II e III.
Vamos resolver por portes:
Afirmativa I: Se a temperatura da fonte fria for de 300 K e se o ciclo apresentar rendimento real correspondente a 75% do rendimento do Ciclo de Carnot associado, então a temperatura da fonte quente será de 750 K, para as condições de projeto.
O rendimento de uma máquina de carnot é dado por:
mu_c= 1- frac{T_f}{T_q}
mu_c= 1- frac{300}{750}=0,6
O rendimento da máquina real será:
mu_R= 0,75times 0,6=0,45
Assertiva correta
rendimento=frac{P_{útil}}{P_{total}}
P_{total}=P_q=frac{P_{útil}}{rendimento}
P_q=frac{15}{0,45}=frac{100}{3},MW
P_f=P_q - P_{útil}=frac{100}{3}- 15=frac{55}{3},MW
Assertiva correta
PtimesDelta{t}=mtimes Q_c
m=frac{PtimesDelta{t}}{Q_c}
m=frac{100times1times7times24times3600}{36times10^{3}}
m=560 toneladas
Portanto, nosso gabarito é a letra E.
Gabarito: E
1889) A passagem de um estado termodinâmico para outro é efetuada através de um caminho que define o tipo de processo entre estes estados. Em relação a tais processos, analise as afirmativas a seguir.
- A) III.
- B) I e II.
- C) I e III.
- D) II e III.
A resposta certa é a letra A) III.
Isso ocorre porque o processo isotérmico é aquele em que a temperatura é mantida constante, o processo isobárico é aquele em que a pressão é mantida constante, e o processo isocórico ou isométrico é aquele em que o volume é mantido constante.
Portanto, apenas a afirmativa III está correta, pois é a única que define corretamente o processo isocórico ou isométrico.
As outras alternativas apresentam combinações incorretas de processos termodinâmicos.
Por exemplo, a alternativa B) afirma que os processos isotérmico e isobárico ocorrem simultaneamente, o que não é verdade. Da mesma forma, as alternativas C) e D) apresentam combinações incorretas de processos.
Portanto, a resposta certa é a letra A) III, que define corretamente o processo isocórico ou isométrico.
The correct answer is A) III.
This occurs because the isothermal process is the one where the temperature is kept constant, the isobaric process is the one where the pressure is kept constant, and the isochoric or isometric process is the one where the volume is kept constant.
Therefore, only statement III is correct, as it is the only one that correctly defines the isochoric or isometric process.
The other alternatives present incorrect combinations of thermodynamic processes.
For example, alternative B) states that the isothermal and isobaric processes occur simultaneously, which is not true. Similarly, alternatives C) and D) present incorrect combinations of processes.
Therefore, the correct answer is A) III, which correctly defines the isochoric or isometric process.
Questão 1890
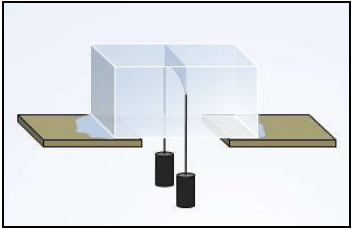
Disponível em: https://docplayer.com.br/43152515-Estados-fisicos-damateria- prof-henrique-dantas.html Acesso em: 15 de novembro de 2021.
Em seguida, o professor pediu que alguns estudantes explicassem o fenômeno observado. Dois estudantes, Lívia e Túlio, tentaram explicar o ocorrido:
Lívia: o gelo, por sofrer um acréscimo de pressão provocado pelo fio, tem a sua temperatura de fusão diminuída e sofre derretimento.
Túlio: O fio, por ser metálico e possuir uma alta condutividade térmica, consegue facilmente aquecer o gelo favorecendo o seu derretimento.
Assinale a alternativa que apresenta as explicações fisicamente CORRETAS:
- A) Somente a de Lívia.
- B) Somente a de Túlio.
- C) As duas estão fisicamente corretas.
- D) As duas estão fisicamente incorretas.
A alternativa correta é letra A) Somente a de Lívia.
A água é uma substância anômala quanto a sua temperatura de fusão (mudança de estado físico da água de sólido para líquido) e, por esse motivo, quando submetida a um aumento de pressão, por exemplo, atmosférica ela se sujeita a uma diminuição da sua temperatura de fusão.
Quando o fio está sujeito a forças como aquelas indicadas na figura, ocorre um aumento de pressão na superfície de contato do fio com a água devido à força de tração do fio sobre a área de contato com o gelo.
A diminuição da temperatura de fusão na área de contato com o gelo leva ao derretimento momentâneo do gelo na região de contato com o fio tracionado. Assim que o arame começa a descer, a pressão e a temperatura voltam ao valor inicial e a água resultante da fusão do gelo, congela novamente.
Desse modo, concluímos que o gabarito é a letra A.
Gabarito: A




