Questões Sobre Termologia - Física - concurso
1891) Um microchip de massa m=2,0 times 10^{-6}g é composto majoritariamente de silício. Durante um minuto de funcionamento, o circuito elétrico do dispositivo dissipa, na forma térmica, uma quantidade de energia Q = 0,96 mJ. Considere que o calor específico do silício é o C_{Si} = 800 J/kgºC. Caso não houvesse nenhum mecanismo de escoamento de calor para fora do dispositivo, em quanto sua temperatura aumentaria após esse tempo de funcionamento?
- A) 4,8 times 101 ºC.
- B) 1,6 times 102 ºC.
- C) 6,0 times 102 ºC.
- D) 1,2 times 103 ºC.
A alternativa correta é letra C) 6,0 times 102 ºC.
Questão de aplicação direta da fórmula de calor, com o cuidado para transformar as unidades de massa.
Alterando o calor específico para grama, temos que ele será C = 0,8 J/gºC e o calor é de 0,96 times 10^{-3} J
Q = m times c times Delta T
0,96 times 10^{-3} = 2 times 10^{-6} times 0,8 times Delta T
Delta T = dfrac{480}{0,8} = 6,0 times 10^2 , ºC
Gabarito: LETRA C.
1892) Para medir a temperatura de um paciente, coloca-se o termômetro debaixo de seu braço (axila) e aguardam-se alguns minutos até que a temperatura do termômetro se iguale à do paciente. Considerando que inicialmente a temperatura do termômetro seja menor que a do paciente, durante esse processo
- A) ocorre transferência de temperatura do corpo do paciente para o termômetro.
- B) ocorre transferência de calor do corpo do paciente para o termômetro.
- C) ocorre transferência de temperatura do termômetro para o corpo do paciente.
- D) ocorre transferência de calor do termômetro para o corpo do paciente.
- E) as quantidades de calor contidas no corpo do paciente e no termômetro se igualam.
A alternativa correta é letra B) ocorre transferência de calor do corpo do paciente para o termômetro.
Temperatura não transfere pessoal.
Questão clássica que tenta confundir o aluno nos conceitos de termodinâmica.
Uma definição simples e eficiente de calor é "energia em fluxo".
Claro que, para que essa energia em fluxo ocorra, temos que ter diferença de temperatura entre o termômetro e a pessoa. Porém, não é a temperatura que flui, e sim, o calor.
Gabarito: LETRA B.
a) ocorre transferência de temperatura do corpo do paciente para o termômetro.
ERRADA. Explicado acima.
c) ocorre transferência de temperatura do termômetro para o corpo do paciente.
ERRADA. Explicado acima.
d) ocorre transferência de calor do termômetro para o corpo do paciente.
ERRADA. Nesse caso, a pessoa aqueceria ainda mais e o termômetro esfriaria.
e) as quantidades de calor contidas no corpo do paciente e no termômetro se igualam.
ERRADA. "quantidade de calor contida" foi uma bela de uma "viajada". O corpo contém temperatura.
1893) Em março de 2020, a Unicamp e o Fermi National Accelerator Laboratory (Fermilab), dos Estados Unidos, assinaram um acordo de cooperação científica com o objetivo de desenvolver tanques para conter argônio líquido a baixíssimas temperaturas (criostatos). Esses tanques abrigarão detectores para o estudo dos neutrinos.
- A) 20 K.
- B) 89 K.
- C) 189 K.
- D) 457 K.
A alternativa correta é letra B) 89 K.
Questão de aplicação direta da transformação de graus Celsius para Kelvin.
T_{Ar} = 273 + (-184) = 89 , K
O enunciado está presente mais a título de curiosidade do que para resolução.
Gabarito: LETRA B.
1894) As recomendações para o preparo ideal do chá branco é aquecer a água à temperatura entre 70ºC a 80ºC. Coloca-se um recipiente de água de 0,3L no fogo, à temperatura ambiente de 25ºC, até que atinja a temperatura de 80ºC. Sabendo que a densidade e o calor específico da água são d = 1,0kg/L e c = 4200,0J/kgºC. A quantidade de calor absorvida pela água para o preparo do chá é
- A) 69,3 × 103J.
- B) 23,1 × 104J.
- C) 100,8 × 103J.
- D) 31,5 × 103J.
A alternativa correta é letra A) 69,3 × 103J.
Pode-se observar que a densidade tem uma relação de 1 para 1 com o volume e massa.
Logo, podemos aplicar diretamente a fórmula de calor
Q = m times c times Delta T
Q = 0,3 times 4.200 times (80-25) = 69.300 = 69,3 times 10^3 , J
Gabarito: LETRA A.
1895) Assinale a alternativa que cita corretamente um processo de transformação da matéria por um fenômeno físico.
- A) Transformação de vinho em vinagre
- B) Preparação de cal a partir do calcário
- C) Enferrujamento de um pedaço de ferro
- D) Queima de um pedaço de papel
- E) Congelamento da água
Resposta: A alternativa correta é a letra E) Congelamento da água.
Explicação:
O congelamento da água é um processo de transformação da matéria por um fenômeno físico, que ocorre quando a temperatura da água é reduzida a 0°C ou abaixo, fazendo com que as moléculas de água sejam ordenadas em uma estrutura cristalina, criando gelo.
Já as outras alternativas não são processos de transformação da matéria por fenômenos físicos:
- A) Transformação de vinho em vinagre é um processo químico, que envolve a oxidação do álcool presente no vinho, transformando-o em ácido acético.
- B) Preparação de cal a partir do calcário é um processo químico, que envolve a queima do calcário para produzir óxido de cálcio.
- C) Enferrujamento de um pedaço de ferro é um processo químico, que envolve a oxidação do ferro em contato com o ar e a umidade.
- D) Queima de um pedaço de papel é um processo químico, que envolve a combustão do papel, liberando calor e produtos químicos.
Portanto, a única alternativa que descreve um processo de transformação da matéria por um fenômeno físico é o congelamento da água.
1896) Assinale a alternativa que cita corretamente o nome do processo que ocorre quando há transmissão ou transferência de calor de um lugar para outro pelo deslocamento de meio material através de correntes que se estabelecem no interior do meio.
- A) Ebulição
- B) Radiação
- C) Sublimação
- D) Convecção
- E) Condução
A alternativa correta é letra D) Convecção.
Convecção é o processo que ocorre quando há transmissão ou transferência de calor de um lugar para outro pelo deslocamento de meio material através de correntes que se estabelecem no interior do meio. Isso acontece quando há uma diferença de temperatura entre dois pontos, fazendo com que as moléculas se movam de uma região de alta temperatura para uma região de baixa temperatura, transferindo calor.
É importante notar que convecção é diferente de condução, que é a transferência de calor entre duas substâncias em contato direto. Convecção envolve o movimento de um fluido (líquido ou gás) que carrega o calor de um lugar para outro.
Um exemplo de convecção é o aquecimento de uma sala por meio de um ventilador que distribui o ar quente uniformemente. Outro exemplo é a formação de correntes oceânicas que transportam calor de uma região do oceano para outra.
Portanto, a alternativa D) Convecção é a resposta correta para a questão.
1897) Kari Kari saiu de sua Terra Indígena Onça, localizada a 50 km da Capital de Roraima, para visitar seu parente em outro Estado do Brasil. Chegando lá, sentiu diferença de temperatura a qual estava acostumado.
- A) 10ºF
- B) 45ºF
- C) 50ºF
- D) 55ºF
- E) 100ºF
A alternativa correta é letra C) 50ºF
Gabarito: LETRA C.
Para encontrar a relação correta entre as escalas termométricas, é preciso conhecer pelo menos 2 pontos em comum. A figura abaixo traz uma relação entre as escalas Celsius, Fahrenheit e Kelvin para alguns pontos como o ponto de fusão e de ebulição da água ao nível do mar:
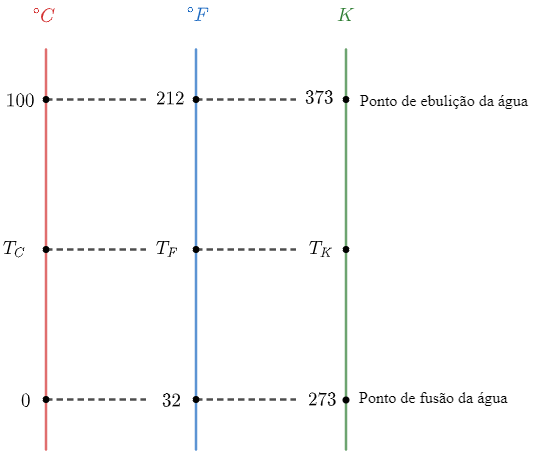
Assim, utilizando a relação de proporção entre as escalas Celsius e Fahrenheit, podemos escrever a equação:
dfrac { T_C - 0 } { 100 - 0 } = dfrac { T_F - 32 } { 212 - 32 }
dfrac { T_C } { 100 } = dfrac { T_F - 32 } { 180 }
dfrac { T_C } { 5 } = dfrac { T_F - 32 } { 9 }
Então, para T_C = 10°C, temos:
dfrac { 10 } { 5 } = dfrac { T_F - 32 } { 9 }
2= dfrac { T_F - 32 } { 9 }
T_F - 32 = 18
T_F = 50 °F
Portanto, a resposta correta é a alternativa (c).
1898) É possível ferver água à temperatura ambiente utilizando uma mangueira com água? Uma pessoa sugere que sim: se deve ter uma coluna vertical de água suficientemente alta feita com uma mangueira. A mangueira está aberta na extremidade mantida em um balde com água na base da coluna, e a outra extremidade é fechada e elevada verticalmente. A mangueira está inicialmente completamente preenchida por água.
- A) V - F - F
- B) F - V - F
- C) F - F - V
- D) F - V - V
Resposta: A) V - F - F
Para entender por que essa é a resposta certa, correta, vamos analisar cada afirmação:
( ) A coluna deve ter pouco mais de 10 m de altura para iniciar a fervura (produção de vapor a partir do líquido com a formação de bolhas) no interior da mangueira, então a coluna desce um pouco e fica estável a uma altura menor e a fervura para.
Essa afirmação está Verdadeira (V). Isso ocorre porque, ao criar uma coluna de água muito alta, a pressão no fundo da coluna aumenta, o que pode causar a água a ferver mesmo à temperatura ambiente. No entanto, quando a água começa a ferver, a coluna desce um pouco e se estabiliza em uma altura menor, o que faz com que a fervura pare.
( ) A coluna deve ter cerca de 10m de altura, mas não há fervura e toda a água irá escorrer pelo tubo até que a mangueira esteja completamente vazia.
Essa afirmação está Falsa (F). Se a coluna tiver cerca de 10m de altura, a pressão no fundo da coluna será suficiente para causar a fervura da água, mesmo à temperatura ambiente.
( ) Não é possível ferver água à temperatura ambiente, na medida em que não há energia térmica suficiente transferida pela gravidade para a água.
Essa afirmação está Falsa (F). Como vimos anteriormente, é possível ferver água à temperatura ambiente utilizando uma coluna de água muito alta, pois a pressão no fundo da coluna aumenta, o que pode causar a fervura da água.
Portanto, a sequência correta de cima para baixo é V - F - F.
1899) Texto associado
- A) O aquário A experimentará uma variação de 60ºC em sua temperatura
- B) O aquário B experimentará uma variação de 60ºC em sua temperatura
- C) O aquário B experimentará 2% a mais de variação em sua temperatura que o aquário A
- D) O aquário A experimentará 2% a mais de variação em sua temperatura que o aquário B
Answer: D) The aquarium A will experience 25% more temperature variation than the aquarium B.
To explain this answer, let's first understand the concept of specific heat capacity. The specific heat capacity of a substance is the amount of heat energy required to raise the temperature of 1 kg of that substance by 1°C. In this problem, we are given that the specific heat capacity of dry air is 1.005 kJ/kg K, and the specific heat capacity of humid air at 80% humidity is 2.5% higher than that of dry air.
Now, let's analyze the situation. We have two aquariums, A and B, with the same mass of air. Aquarium A has dry air, and aquarium B has humid air at 80% humidity. Both aquariums are heated by a 100 W heat source for 1 hour. We need to find out which aquarium will experience a greater temperature variation.
Since the specific heat capacity of humid air is higher than that of dry air, it means that humid air can absorb more heat energy without a significant increase in temperature. Therefore, the temperature variation in aquarium B, which has humid air, will be less than that in aquarium A, which has dry air.
However, the question asks us to find out which aquarium will experience a greater temperature variation. Since aquarium A has dry air, which has a lower specific heat capacity, it will experience a greater temperature variation than aquarium B. Therefore, the correct answer is D) The aquarium A will experience 25% more temperature variation than the aquarium B.
This answer makes sense because the humid air in aquarium B can absorb more heat energy without a significant increase in temperature, whereas the dry air in aquarium A will experience a greater temperature variation due to its lower specific heat capacity.
Questão 1900

Se o calor específico da água é de 1 cal /goC, a admitindo que a fusão do gelo ocorre a 0 ºC. Assinale a alternativa que apresenta o valor que identifica corretamente o valor do calor latente do gelo obtido pelo experimento do professor.
- A) 80,0 cal/g
- B) 82,7 cal/g
- C) 83,2 cal/g
- D) 84,3 cal/g
A alternativa correta é letra B) 82,7 cal/g
Para encontrar o valor do calor latente do gelo, precisamos analisar a situação experimental apresentada. O professor congela 1 volume de copo americano de água e, em seguida, adiciona 3 volumes de copo americano de água quente a 80,5°C. A mistura é então isolada termicamente e o termômetro indica que o equilíbrio térmico é alcançado a 39,7°C.
Para resolver esse problema, podemos utilizar a fórmula de mistura de calor:
$$Q = mcDelta T$$
Onde:
- $Q$ é o calor transferido;
- $m$ é a massa da substância;
- $c$ é o calor específico da substância;
- $Delta T$ é a variação de temperatura.
No caso da água quente, temos:
$$Q_1 = 3m times 1 frac{text{cal}}{text{g}^{circ}text{C}} times (80,5 - 39,7)^{circ}text{C} = 121,2 m text{ cal}$$
Já para o gelo, temos:
$$Q_2 = m times L_f times (0 - 39,7)^{circ}text{C} = -m times L_f times 39,7^{circ}text{C}$$
Onde $L_f$ é o calor latente de fusão do gelo.
Como o sistema está em equilíbrio térmico, o calor liberado pela água quente é igual ao calor absorvido pelo gelo:
$$Q_1 = -Q_2$$
Substituindo as expressões anteriormente encontradas, temos:
$$121,2 m text{ cal} = m times L_f times 39,7^{circ}text{C}$$
Dividindo ambos os lados pela massa $m$, obtemos:
$$L_f = frac{121,2}{39,7} frac{text{cal}}{text{g}} = 82,7 frac{text{cal}}{text{g}}$$
Portanto, a alternativa correta é a letra B) 82,7 cal/g.
