Questões Sobre Termologia - Física - concurso
2011) Considere um tubo cilíndrico feito com um material de coeficiente de dilatação linear a com um líquido de coeficiente de dilatação volumétrica β.
- A) 2
- B) 1
- C) 1/2
- D) 1/3
- E) 1/4
A alternativa correta é letra C) 1/2
Pessoal, na variação volumétrica teremos
V = V_0 + V_0 beta Delta T
Como no volume final, ele quer a mesma altura (e trocando o volume por termos de área e altura), temos
A_{final} h = A_{inicial} h + A_{inicial} h beta Delta T
A_{final} = A_{inicial} + A_{inicial} beta Delta T
Agora pessoal, sabemos que o coeficiente de dilatação da área é dado por
A_{final} = A_{inicial} + A_{inicial} 2 alpha Delta T
Logo,
A_{inicial} + A_{inicial} 2 alpha Delta T = A_{inicial} + A_{inicial} beta Delta T
2 alpha = beta
dfrac{alpha}{beta} = dfrac{1}{2}
Gabarito: LETRA C.
Questão 2012
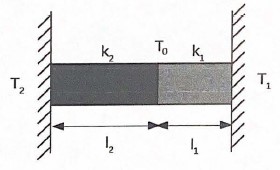
Considerando que o lado direito está em equilíbrio térmico, à temperatura T1 = 0ºC, que o lado esquerdo está a T2 = 100 ºC, que o fluxo de calor se dá em regime estacionário e que não há trocas de calor ao longo da superfície lateral das barras, detennine a temperatura T0 na junção das barras.
- A) 12 ºC
- B) 20 ºC
- C) 25 ºC
- D) 30 ºC
- E) 35 ºC
A alternativa correta é letra C) 25 ºC
Pessoal, o fluxo de calor em uma barra assim é igual para todos os pontos dela.
Logo, mesmo mudando a barra, o fluxo que é dado pela equação abaixo permanece igual em qualquer ponto.
phi = dfrac{k A (T_2-T_1)}{L}
Obviamente, pegaremos os pontos que abrangem a temperatura no ponto intermediário da barra.
Partindo da esquerda para direita (mais quente para o mais frio), temos
dfrac{k_2 A (T_2-T_0)}{L_2} = dfrac{k_1 A (T_0-T_1)}{L_1}
dfrac{200 (100 - T_0)}{2} = dfrac{300 (T_0 - 0)}{1}
100 - T_0 = 3 T_0
T_0 = 25 , ºC
Gabarito: LETRA C.
Questão 2013
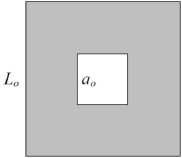
A figura representa uma placa quadrada de alumínio, de lado Lo, que possui um furo, também quadrado, de lado ao. Essa placa passa por processo de aquecimento, dilatando-se até um valor L > Lo. Nesse processo,
- A) ao diminui e a densidade da placa aumenta.
- B) ao diminui e a densidade da placa diminui.
- C) ao aumenta e a densidade da placa aumenta.
- D) ao aumenta e a densidade de placa diminui.
Resposta:
A resposta correta é a letra D) $a_o$ aumenta e a densidade da placa diminui.
Explicação:
Quando a placa de alumínio é submetida a um processo de aquecimento, ela se dilata. Isso significa que as partículas do material se afastam umas das outras, ocupando um volume maior. Como resultado, a densidade do material diminui. Além disso, como o lado da placa $L_o$ aumenta para $L > L_o$, a distância entre as partículas também aumenta, contribuindo para a diminuição da densidade.
Portanto, a afirmação "a densidade da placa aumenta" é incorreta. A densidade da placa diminui devido à dilatação do material durante o processo de aquecimento.
As outras opções apresentadas são inconsistentes com a física do processo de aquecimento. A opção A) é impossível, pois a densidade não pode aumentar se o material se dilata. A opção B) também é errada, pois a densidade não pode diminuir se o lado da placa diminui. A opção C) é igualmente incorreta, pois a densidade não pode aumentar se o lado da placa aumenta.
Em resumo, a resposta correta é a letra D) $a_o$ aumenta e a densidade da placa diminui, pois a dilatação do material durante o processo de aquecimento leva a uma diminuição na densidade.
2014) Um pequeno vasilhame com 10,0 g de água a 20,0 ºC é colocado em um congelador. Após algum tempo, essa água se transforma em um pequeno bloco de gelo a uma temperatura de –20 ºC. Considere que o calor específico da água é de 1,0 cal/g ºC, que o calor específico do gelo é de 0,5 cal/g ºC e que o calor latente de fusão do gelo é de 80 cal/g. A quantidade de calor, em calorias, retirada do sistema (água/gelo) durante todo esse processo foi de
- A) 200 cal.
- B) 400 cal.
- C) 800 cal.
- D) 1100 cal.
Resposta: D) 1100 cal.
Para resolver essa questão, precisamos calcular a quantidade de calor retirada do sistema (água/gelo) durante todo o processo de transformação da água em gelo.
Primeiramente, vamos calcular a quantidade de calor necessária para reduzir a temperatura da água de 20,0°C para 0°C. Isso é feito utilizando a fórmula Q = mcΔT, onde Q é a quantidade de calor, m é a massa da água (10,0 g), c é o calor específico da água (1,0 cal/g°C) e ΔT é a variação de temperatura (20,0°C para 0°C). Substituindo os valores, obtemos:
$$Q_1 = mcDelta T = 10,0 text{ g} times 1,0 frac{text{cal}}{text{g°C}} times (-20,0°C) = -200 text{ cal}$$Em seguida, precisamos calcular a quantidade de calor necessária para congelar a água a 0°C. Isso é feito utilizando a fórmula Q = mL, onde Q é a quantidade de calor, m é a massa da água (10,0 g) e L é o calor latente de fusão do gelo (80 cal/g). Substituindo os valores, obtemos:
$$Q_2 = mL = 10,0 text{ g} times 80 frac{text{cal}}{text{g}} = 800 text{ cal}$$Finalmente, precisamos calcular a quantidade de calor necessária para reduzir a temperatura do gelo de 0°C para -20,0°C. Isso é feito utilizando a fórmula Q = mcΔT, onde Q é a quantidade de calor, m é a massa do gelo (10,0 g), c é o calor específico do gelo (0,5 cal/g°C) e ΔT é a variação de temperatura (0°C para -20,0°C). Substituindo os valores, obtemos:
$$Q_3 = mcDelta T = 10,0 text{ g} times 0,5 frac{text{cal}}{text{g°C}} times (-20,0°C) = -100 text{ cal}$$Agora, somamos as quantidades de calor calculadas anteriormente para obter a quantidade total de calor retirada do sistema:
$$Q_{total} = Q_1 + Q_2 + Q_3 = -200 text{ cal} + 800 text{ cal} - 100 text{ cal} = 1100 text{ cal}$$Portanto, a alternativa correta é D) 1100 cal.
2015) A fusão é uma mudança de estado em que uma substância passa do estado sólido para o estado líquido, ao passo que a ebulição é uma passagem do estado líquido para o gasoso. Os processos inversos são chamados, respectivamente, de solidificação e condensação. Em relação a esses processos,
- A) se um líquido se encontra em seu ponto de ebulição, não é mais necessário fornecer calor a ele para que o processo seja mantido até o final.
- B) a uma dada pressão, a temperatura na qual ocorre a fusão de uma substância não se altera.
- C) a quantidade de calor que deve ser retirada de uma substância, por unidade de massa, para que ocorra sua solidificação, é denominada de calor específico de solidificação.
- D) durante a ebulição, apesar de continuar fornecendo calor ao líquido, sua temperatura permanece constante e o vapor que vai se formando encontra-se em temperatura maior que a do líquido.
A resposta correta é a letra B) "a uma dada pressão, temperatura na qual ocorre a fusão de uma substância não se altera."
Para entender melhor essa resposta, vamos analisar os processos de mudanças de estado. A fusão é a mudança de estado em que uma substância passa do estado sólido para o estado líquido, ao passo que a ebulição é a passagem do estado líquido para o gasoso. Já os processos inversos são chamados, respectivamente, de solidificação e condensação.
No caso da letra A, está errado, pois quando um líquido se encontra em seu ponto de ebulição, não é necessário fornecer calor para que o processo seja mantido até o final. Além disso, a temperatura do líquido permanece constante durante a ebulição.
Já a letra C está relacionada ao calor específico de solidificação, que é a quantidade de calor que deve ser retirada de uma substância, por unidade de massa, para que ocorra sua solidificação.
A letra D também está errada, pois durante a ebulição, apesar de continuar fornecendo calor ao líquido, sua temperatura permanece constante e o vapor que vai se formando encontra-se em temperatura maior que a do líquido.
Portanto, a resposta correta é a letra B, pois a temperatura de fusão de uma substância não se altera com a pressão. Isso significa que, independentemente da pressão aplicada, a temperatura em que ocorre a fusão de uma substância é sempre a mesma.
Essa propriedade é importante em various processos físicos e químicos, como por exemplo, na determinação das propriedades termodinâmicas de uma substância.
2016) Considere uma cascata de 210 m de altura. A água cai de seu ponto mais alto com velocidade desprezível. Suponha uma quantidade de água equivalente a 200 kg colidindo com o solo e que toda a energia cinética que essa água adquire tenha se convertido em calor, aquecendo essa mesma massa de água. Considere todos os atritos e resistências do ar desprezíveis, que a aceleração gravitacional é de 10 m/s2, que o calor específico da água vale c = 1,0 cal/g ºC e que 1 cal = 4,2 J. Nessa situação hipotética, a variação de temperatura dessa quantidade de água seria de
- A) 0,21 ºC.
- B) 0,40 ºC.
- C) 0,50 ºC.
- D) 0,88 ºC.
A resposta certa é a letra C) 0,50 ºC.
Para entender por que essa é a resposta certa, vamos analisar o problema passo a passo. Temos uma cascata de 210 m de altura, e uma quantidade de água equivalente a 200 kg que cai de seu ponto mais alto com velocidade desprezível. Quando essa água colide com o solo, toda a energia cinética que ela adquiriu se converte em calor, aquecendo a mesma massa de água.
Podemos calcular a energia cinética da água usando a fórmulaEk = m * g * h, onde Ek é a energia cinética, m é a massa da água (200 kg), g é a aceleração gravitacional (10 m/s²) e h é a altura da cascata (210 m). Substituindo os valores, obtemos:
Ek = 200 kg * 10 m/s² * 210 m = 42.000 J
Como toda a energia cinética se converte em calor, podemos calcular a variação de temperatura da água usando a fórmula ΔT = Ek / (m * c), onde ΔT é a variação de temperatura, m é a massa da água (200 kg) e c é o calor específico da água (1,0 cal/g ºC). Substituindo os valores, obtemos:
ΔT = 42.000 J / (200 kg * 1,0 cal/g ºC * 4,2 J/cal) = 0,50 ºC
Portanto, a variação de temperatura da água seria de 0,50 ºC.
2017) O rótulo em uma lata pressurizada de desodorante spray adverte contra o aquecimento da lata acima de 130 ºF. Em graus Celsius, esta temperatura é
- A) 54.
- B) 90.
- C) 98.
- D) 115.
- E) 122.
A alternativa correta é letra A) 54.
Gabarito: LETRA A.
Para encontrar uma relação entre duas escalas, é preciso conhecer pelo menos 2 pontos em comum entre elas. Sabemos que a fusão do gelo ocorre em 0°C, o que equivale a 32°F, e a vaporização da água ocorre em 100°C, correspondente a 212°F. Assim, podemos estabelecer uma relação entre as duas escalas como nos mostra a figura a seguir:
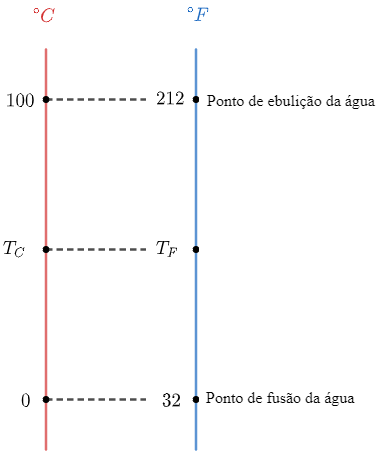
Assim, utilizando a relação de proporção entre as escalas Celsius e Fahrenheit, podemos escrever a equação:
dfrac { T_C - 0 } { 100 - 0 } = dfrac { T_F - 32 } { 212 - 32 }
dfrac { T_C } { 100 } = dfrac { T_F - 32 } { 180 }
dfrac { T_C } { 5 } = dfrac { T_F - 32 } { 9 }
T_C = 5 cdot dfrac { T_F - 32 } { 9 }
Então, para T_F = 130°F, temos:
T_C = 5 cdot dfrac { 130 - 32 } { 9 }
T_C = 5 cdot dfrac { 98 } { 9 }
T_C approx 54°C
Portanto, a resposta correta é a alternativa (a).
2018) Uma barra de ferro foi aquecida de 30 ºC a 80 ºC. O comprimento final da barra após esse aquecimento ficou em 115 cm. Considerando que o coeficiente de expansão linear do ferro seja 3×10–3 ºC–1, a variação no comprimento da barra de ferro após esse aquecimento foi de:
- A) 0,015 %.
- B) 0,15%.
- C) 1,5 %.
- D) 15 %.
- E) 150 %.
A alternativa correta é letra D) 15 %.
Gabarito: LETRA D.
Para determinar a variação no comprimento da barra de ferro, podemos usar a equação da dilatação linear, que é dada por:
Delta L = alpha L_0 Delta T tag 1
Onde:
- Delta L é a variação no comprimento da barra;
- alpha é o coeficiente de expansão linear do ferro;
- L_0 é o comprimento inicial da barra;
- Delta T é a variação de temperatura.
Como a variação no comprimento da barra é dada em porcentagem nas alternativas, precisamos usar a fórmula:
text{Variação percentual} = dfrac { Delta L } { L_0 } cdot 100 tag 2
Da equação (1), temos:
Delta L = alpha L_0 Delta T
dfrac { Delta L } { L_0 } = alpha Delta T
Substituindo os valores do enunciado, temos:
dfrac { Delta L } { L_0 } = 3 times 10^{-3} cdot left( 80 - 30 right)
dfrac { Delta L } { L_0 } = 0,15
Então, da equação (2), temos:
text{Variação percentual} = dfrac { Delta L } { L_0 } cdot 100
text{Variação percentual} = 0,15 cdot 100
text{Variação percentual} = 15 %
Portanto, a resposta correta é a alternativa (d).
2019) A quantidade de calor necessária para elevar a temperatura de 1,0 Kg de uma substância por um Kelvin é:
- A) a capacidade térmica.
- B) o calor específico.
- C) o calor latente.
- D) o calor fundente.
- E) a caloria.
A alternativa correta é letra B) o calor específico.
Gabarito: LETRA B.
Calor é a forma de energia térmica que se desloca de um corpo para outro devido à diferença de temperatura entre eles. Nesse contexto, existem duas formas de se categorizá-lo: calor sensível e calor latente.
O calor sensível está relacionado à mudança de temperatura de uma substância sem ocorrer mudança de fase. É a energia térmica transferida que resulta em um aumento ou diminuição na temperatura do material. Esse tipo de calor está diretamente relacionado ao calor específico da substância, uma propriedade física que indica a quantidade de energia térmica necessária para elevar a temperatura de uma certa quantidade de substância em uma unidade de temperatura.
Dessa forma, podemos afirmar que a quantidade de calor necessária para elevar a temperatura de 1,0 Kg de uma substância por um Kelvin, como o enunciado menciona, corresponde ao calor específico da substância.
Por outro lado, o calor latente está associado à mudança de fase de uma substância, como a fusão, a vaporização e a solidificação. Durante essas transições de fase, a temperatura permanece constante enquanto a energia térmica é absorvida ou liberada pela substância para mudar seu estado físico. O calor latente é determinado pelo calor específico de transformação da substância, como o calor latente de fusão ou o calor latente de vaporização.
A capacidade térmica é uma propriedade física de um objeto ou substância que mede sua capacidade de absorver ou liberar calor. Ela está relacionada à quantidade de calor que um objeto pode armazenar ou trocar em resposta a uma variação de temperatura.
A capacidade térmica e o calor específico estão relacionados, mas representam conceitos diferentes. O calor específico é uma propriedade específica de cada substância que indica a quantidade de calor necessária para aquecer uma determinada massa dessa substância, enquanto a capacidade térmica é uma propriedade do objeto ou sistema como um todo, que leva em conta tanto a massa do objeto quanto seu calor específico.
Portanto, a resposta correta é a alternativa (b).
2020) Uma chaleira elétrica é preenchida com 500 g de água e está inicialmente a uma temperatura de 15 ºC. A chaleira tem uma potência de 2 kW. Considerando que o calor específico da água é 4.180 JKg–1K–1, o tempo necessário para a chaleira aquecer a água até 100 ºC é:
- A) 2,5 horas.
- B) 1,5 horas.
- C) 25 minutos.
- D) 15 minutos.
- E) 1,5 minuto.
A alternativa correta é letra E) 1,5 minuto.
Gabarito: LETRA E.
Para determinar o tempo necessário para a chaleira aquecer a água até 100 °C, primeiro vamos calcular a quantidade de calor fornecida para o aumento de temperatura:
Q = m c Delta T
Onde m é a massa, c o calor específico e Delta T a variação de temperatura.
Do enunciado, temos que m = 500, g = 0,5 , kg, c = 4180 , J/kg cdot K e Delta T = 100 - 15 = 85 °C. Como a variação de temperatura em Kelvin é igual à variação de temperatura em graus Celsius, o calor é dado por:
Q = 0,500 cdot 4180 cdot 85
Q = 177650 , J
Q = 177,65 , kJ
A potência da chaleira corresponde a sua taxa de transferência de energia, que é dada por:
P = dfrac Q { Delta t }
Onde:
- P é a potência (P = 2 ,kW neste caso)
- Q é a quantidade de calor (Q = 177,65 ,kJ)
- Delta t é o tempo necessário para aquecer a água (em segundos, já que 1 , W = 1 , J / 1 , s.
Reorganizando a equação da potência, podemos encontrar o tempo:
Delta t = dfrac QP
Logo,
Delta t = dfrac { 177,65 } { 2 }
Delta t approx 89 , s
Delta t approx 1 , min , 29 , s
Delta t approx 1,5 , min
Portanto, a resposta correta é a alternativa (e).
