Questões Sobre Termologia - Física - concurso
2141) Um estudante de ciências realiza um experimento fazendo uso de uma fonte térmica que é capaz de fornecer, de forma lenta, calor a um bloco de gelo mantido inicialmente a -10 °C. Ao final de seu experimento, o estudante obteve como resultado vapor de água a 100 °C. Para tal resultado ser possível, é necessário gerar mudanças de temperatura e mudanças de estados de agregação da matéria. Assim, é correto afirmar que a sequência de calores envolvidos durante o experimento é:
- A) latente, sensível e latente.
- B) sensível, latente, sensível e latente.
- C) latente, sensível, latente e sensível.
- D) sensível, latente e sensível.
Resposta: A alternativa correta é B) sensível, latente, sensível e latente.
Para entender porque essa alternativa é correta, vamos analisar o experimento realizado pelo estudante de ciências.
Inicialmente, o bloco de gelo está a -10°C, o que significa que a água está no estado sólido. Quando a fonte térmica começa a fornecer calor ao bloco de gelo, a temperatura do gelo começa a subir.
Quando a temperatura do gelo alcança 0°C, o gelo começa a derreter, transformando-se em água líquida. Nesse processo, ocorre uma mudança de estado de agregação da matéria, da fase sólida para a fase líquida. Esse processo é chamado de fusão e requer uma quantidade de calor conhecida como calor latente de fusão.
À medida que a água líquida continua a absorver calor, a temperatura da água começa a subir novamente. Quando a temperatura da água alcança 100°C, a água começa a evaporar, transformando-se em vapor de água. Nesse processo, ocorre outra mudança de estado de agregação da matéria, da fase líquida para a fase gasosa. Esse processo é chamado de vaporização e também requer uma quantidade de calor conhecida como calor latente de vaporização.
Portanto, durante o experimento, ocorreram dois processos que envolveram mudanças de estado de agregação da matéria e absorção de calor. O primeiro processo foi a fusão do gelo, que requer calor latente, e o segundo processo foi a vaporização da água, que também requer calor latente.
Além disso, também ocorreram mudanças de temperatura da água, que absorveu calor sensível para aumentar sua temperatura.
Portanto, a sequência correta de calores envolvidos durante o experimento é: sensível, latente, sensível e latente.
Essa sequência é representada pela alternativa B) sensível, latente, sensível e latente.
2142) Uma substância pura pode se apresentar em três estados de agregação: sólido, líquido e gasoso. Com relação às mudanças de fase à pressão constante de uma determinada substância pura, podemos afirmar que:
- A) o calor latente de fusão é trocado quando a substância tem a sua temperatura diminuída durante a transformação de líquido para sólido.
- B) o calor latente de vaporização é trocado quando a substância tem a sua temperatura aumentada durante a transformação de vapor para líquido.
- C) o calor específico da substância no estado líquido e o calor específico da substância no estado de vapor são iguais.
- D) a capacidade térmica da substância no estado sólido e a capacidade térmica da substância no estado líquido são iguais.
- E) a razão entre o calor trocado e a variação de temperatura durante o aquecimento, no estado sólido, depende da massa da substância.
A alternativa correta é letra E) a razão entre o calor trocado e a variação de temperatura durante o aquecimento, no estado sólido, depende da massa da substância.
Vamos verificar afirmativa por afirmativa.
a) o calor latente de fusão é trocado quando a substância tem a sua temperatura diminuída durante a transformação de líquido para sólido.
ERRADO. Pessoal, em substâncias puras não temos variação de temperatura durante a troca de estado.
b) o calor latente de vaporização é trocado quando a substância tem a sua temperatura aumentada durante a transformação de vapor para líquido.
ERRADO. Pessoal, em substâncias puras não temos variação de temperatura durante a troca de estado.
c) o calor específico da substância no estado líquido e o calor específico da substância no estado de vapor são iguais.
ERRADO. O calor específico varia a depender do estado da substância (sólido, líquido ou gasoso).
d) a capacidade térmica da substância no estado sólido e a capacidade térmica da substância no estado líquido são iguais.
ERRADO. A capacidade térmica varia a depender do estado da substância (sólido, líquido ou gasoso).
e) a razão entre o calor trocado e a variação de temperatura durante o aquecimento, no estado sólido, depende da massa da substância.
CORRETA. Segue,
Q = m c Delta T
dfrac{Q}{Delta T} = m c
2143) Em um recipiente contendo certa quantidade de água a 20ºC é imerso um bloco A, inicialmente à temperatura de 90ºC. Em outro recipiente, contendo a mesma quantidade de água à mesma temperatura de 20ºC, é imerso outro bloco, B, também à temperatura de 90ºC. Sabe-se que a medida da capacidade térmica do bloco A é o dobro da medida da capacidade térmica do bloco B. Desprezando-se as perdas de calor, ao se atingir o equilíbrio térmico em ambas as situações, analise as afirmativas abaixo.
- A) Apenas as afirmativas I e II.
- B) Apenas as afirmativas I e III.
- C) Apenas as afirmativas II e III.
- D) As Afirmativas I, II e III.
- E) Apenas a afirmativa II.
A alternativa correta é letra A) Apenas as afirmativas I e II.
Vamos verificar afirmativa por afirmativa.
CORRETA. Como temos
Q = m_A c_A Delta T_A
Q = m_B c_B Delta T_B
c_A > c_B
Aqui, Q é o calor "roubado" pelo recipiente com água. Como a capacidade c de A é maior, sua variação de temperatura Delta T é menor. Logo, ele conseguirá "segurar" sua temperatura a um patamar mais alto que B, que resfriará mais.
CORRETA. Pessoal, já explicado na anterior.
Como a capacidade c de B é menor, significa que sua variação será maior (são inversamente proporcionais).
Com isso, ele vai ser "resfriado mais" do que o A.
ERRADA. Os dois recebem a mesma quantidade de calor Q. O que difere, é a forma como eles se resfriam com o mesmo calor fornecido.
Gabarito: LETRA A.
2144) Um termistor é um dispositivo eletrônico, em estado sólido, cuja principal característica é a rápida variação da resistência elétrica com a temperatura. A resistência R pode ser descrita na forma R = R0eB/T, sendo R0 e B constantes características do termistor em questão, em Ohms e Kelvin, respectivamente, e T a temperatura do dispositivo. Suponha que um laboratório de física possui apenas termômetros na escala Réaumur, expressa em ºR. A uma temperatura de 48ºR, a resistência do termistor é R1 Omega, e, a uma temperatura de 80ºR, a resistência do termistor é R2 Omega. Assim, assinale a opção que apresenta a variação DeltaR = R2 – R1 para essa variação de temperatura, expressa em termos de R0 e B.
- A) R0(eB/373 – eB/333)
- B) R0(eB/353 – eB/321)
- C) R0(eB/80 – eB/48)
- D) R0eB/32
- E) R0eB/40
A alternativa correta é letra A) R0(eB/373 – eB/333)
Pessoal, o primeiro passo nosso é a transformação de Kelvin para a temperatura em R.
Precisamos fazer isso por meio de interpolação com as temperaturas fornecidas envolvendo a água.
dfrac{80 - 0 }{ 373 - 273} = dfrac{R - 0}{K - 273}
dfrac{80 }{100} = dfrac{R}{K - 273}
K = 273 + dfrac{5 R}{4}
Aplicando agora para 48 e 80 R,
K = 273 + dfrac{5 times 48}{4} = 333K
K = 273 + dfrac{5 times 80}{4} = 373 K
Finalmente,
Delta R = R_2 - R_1
Delta R = R_0 e^{B/373} - R_0 e^{B/333}
Gabarito: LETRA A.
2145) O custo com a refrigeração de um ambiente é aproximadamente proporcional à taxa com que o calor é absorvido pelo ambiente dividida pelo coeficiente de desempenho (CD) do ar-condicionado. Uma sala de aula possui ar-condicionado e apenas uma das quatro paredes da sala, que possui área A, espessura L e condutividade térmica k, recebe sol diretamente. Em um dia típico de calor, a temperatura do lado externo dessa parede é de 38ºC. Em um instante inicial (t1), a temperatura do ar dentro da sala de aula está em 18ºC. Em seguida, 25 alunos entram na sala emitindo calor, cada um, a uma taxa de 100W. Após um certo tempo, no instante t2, o ar do ambiente atinge novamente o equilíbrio térmico a 18ºC. Desprezando as trocas de calor do ambiente interno da sala com o piso, com o teto e com as outras três paredes e considerando que entre os instantes t1 e t2 a temperatura externa se manteve constante e que nenhum aluno entrou ou saiu da sala, é correto afirmar que o custo com a refrigeração no instante t2 será:
- A) 5 vezes maior do que no instante t1.
- B) 6 vezes maior do que no instante t1.
- C) 25 vezes maior do que no instante t1.
- D) 100 vezes maior do que no instante t1.
- E) igual ao do instante t1.
A alternativa correta é letra B) 6 vezes maior do que no instante t1.
Pessoal, vamos calcular o fluxo de calor dos alunos e da parede.
Q_{alunos} = 100 times 25 = 2.500 , W
Q_{parede} = dfrac{ U A Delta T}{L} = dfrac{0,1 times 50 times (38 - 28)}{20 times 10^{-3}} = 500 , W
Q_{total} = 500 + 2.500 = 3.000 , W
Agora, a relação entre eles é (reparem que o CD = 3 não influi pois será eliminado)
dfrac{Q_{total}}{Q_{parede}} = dfrac{3.000/6}{500/6} = 6
Gabarito: LETRA B.
Questão 2146
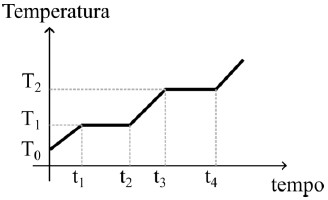
Indique a alternativa correta:
- A) Entre os tempos t1 e t2, a substância está passando por uma transição de fase chamada de ebulição.
- B) Entre os tempos t2 e t3 a substância está mudando da fase sólida para a fase líquida.
- C) Entre os tempos t3 e t4 somente existe uma fase da substância.
- D) Numa mesma fase, a quantidade de calor trocada para aumentar sua temperatura é chamada de calor latente.
- E) Entre os tempos t3 e t4 coexistem as fases líquida e gasosa da substância.
Resposta: A alternativa correta é a letra E) Entre os tempos t3 e t4, coexistem as fases líquida e gasosa da substância.
Explicação: Ao analisar o gráfico, fornecido, podemos observar que a energia está sendo constantemente transferida para a substância em forma de calor ao longo do tempo. Isso significa que a substância está absorvendo calor e mudando de fase.
No gráfico, podemos ver que entre os tempos t1 e t2, a substância está mudando de fase, provavelmente de sólida para líquida, pois a temperatura aumenta gradualmente.
Entre os tempos t2 e t3, a temperatura se mantém constante, o que indica que a substância está mudando de fase, provavelmente de líquida para gasosa.
Finalmente, entre os tempos t3 e t4, a temperatura se mantém constante novamente, o que indica que coexistem as fases líquida e gasosa da substância. Portanto, a alternativa correta é a letra E).
É importante notar que a transferência de calor não é necessariamente uma mudança de fase. A mudança de fase ocorre quando a substância alcança um ponto específico de temperatura, conhecido como ponto de fusão ou ponto de ebulição, dependendo do tipo de mudança de fase.
No caso do gráfico fornecido, a substância está mudando de fase de líquida para gasosa entre os tempos t2 e t3, e coexistem as fases líquida e gasosa entre os tempos t3 e t4.
2147) Na escala de temperatura Fahrenheit, o ponto de fusão da água corresponde a 32 °F, enquanto o ponto de ebulição da água corresponde a 212 °F. Na escala de temperatura Celsius, esses pontos correspondem, respectivamente, a 0 °C e 100 °C.
- A) A temperatura de 212 °F é maior que 100 °C.
- B) A temperatura de 0 °F corresponde a −32 °C.
- C) Se a temperatura corporal de uma pessoa atingir 3 dígitos na escala Fahrenheit, então essa pessoa estará, pelo menos, no estado febril.
- D) Os termômetros de Belém do Pará, durante o verão, comumente atingem a temperatura de 0 °F.
- E) Uma pessoa com temperatura corporal de 122 °F estará no estado normal.
A alternativa correta é letra C) Se a temperatura corporal de uma pessoa atingir 3 dígitos na escala Fahrenheit, então essa pessoa estará, pelo menos, no estado febril.
Gabarito: LETRA C.
Para encontrar uma relação entre escalas, é preciso conhecer pelo menos 2 pontos em comum entre elas. Como o enunciado menciona, a fusão do gelo ocorre em 0°C, o que equivale a 32°F, e a vaporização da água ocorre em 100°C, correspondente a 212°F. Assim, podemos estabelecer uma relação entre as duas escalas como nos mostra a figura a seguir:
Então, utilizando a relação de proporção entre as escalas, podemos escrever uma equação geral de conversão entre elas:
dfrac { T_C - 0 } { 100 - 0 } = dfrac { T_F -32 } { 212 - 32 }
dfrac { T_C } { 100 } = dfrac { T_F -32 } { 180 }
dfrac { T_C } { 5 } = dfrac { T_F -32 } { 9 } tag 1
Assim, vamos analisar cada uma das alternativas:
a) A temperatura de 212 °F é maior que 100 °C.
Incorreta. Como mencionado, 212 °F corresponde ao ponto de ebulição da água na escala Fahrenheit, o que equivale a 100 °C. Logo, as temperaturas são iguais.
b) A temperatura de 0 °F corresponde a −32 °C.
Incorreta. Substituindo T_F = 0°F na equação (1), temos:
dfrac { T_C } { 5 } = dfrac { 0 -32 } { 9 }
dfrac { T_C } { 5 } = -dfrac { 32 } { 9 }
T_C = - 5 cdot dfrac { 32 } { 9 }
T_C approx - 17,77 , °C
Ou seja, 0 °F corresponde a aproximadamente -17,77 °C.
c) Se a temperatura corporal de uma pessoa atingir 3 dígitos na escala Fahrenheit, então essa pessoa estará, pelo menos, no estado febril.
Correta. Substituindo T_F = 100°F na equação (1), temos:
dfrac { T_C } { 5 } = dfrac { 100 -32 } { 9 }
dfrac { T_C } { 5 } = dfrac { 68 } { 9 }
T_C = 5 cdot dfrac { 68 } { 9 }
T_C approx 37,77 , °C
Logo, a temperatura de 100 °F corresponde a aproximadamente 37,8 °C. Então, de acordo com a tabela do enunciado, se a temperatura corporal de uma pessoa atingir 3 dígitos na escala Fahrenheit (100 °F), então essa pessoa estará, pelo menos, no estado febril.
d) Os termômetros de Belém do Pará, durante o verão, comumente atingem a temperatura de 0 °F.
Incorreta. Belém do Pará tem um clima tropical úmido, onde as temperaturas raramente caem abaixo de 20 °C, mesmo durante o inverno. Como mencionado, 0 °F corresponde a aproximadamente -17,77 °C. A temperatura de 0 °F é extremamente baixa e não é alcançada em Belém do Pará.
e) Uma pessoa com temperatura corporal de 122 °F estará no estado normal.
Incorreta. Substituindo T_F = 122°F na equação (1), temos:
dfrac { T_C } { 5 } = dfrac { 122 -32 } { 9 }
dfrac { T_C } { 5 } = dfrac { 90 } { 9 }
dfrac { T_C } { 5 } = 10
T_C = 5 cdot 10
T_C = 50 , °C
Ou seja, 122 °F corresponde a 50 °C, o que está muito acima do estado normal da temperatura corporal humana.
Portanto, a resposta correta é a alternativa (c).
2148) Calor é energia transferida (cedida ou recebida) pelas substâncias em função da diferença da temperatura. O calor específico de um corpo é a quantidade de calor que uma substância necessita para variar sua temperatura em 1ºC para cada grama da substância. O calor específico da água é justamente 1 cal/(g ºC). (1 cal = 1 caloria = 4,184J)
- A) 400 g de água de 20 °C para 70 °C, a água necessitaria receber mais que 8 kcal.
- B) 1 kg de água em 10 °C, seriam necessárias 1 kcal.
- C) 10 g de água de 30 °C para 10 °C, a água necessitaria receber 200 cal de calor.
- D) 200 g de água de 20 °C para 40 °C, a água necessitaria receber 400 cal de calor.
- E) 200 g de água de 50 °C para 10 °C, a água necessitaria ceder menos que 4 kcal de calor.
A alternativa correta é letra A) 400 g de água de 20 °C para 70 °C, a água necessitaria receber mais que 8 kcal.
Gabarito: LETRA A.
A quantidade de calor fornecida a um corpo que gera apenas variações de temperatura, sem produzir mudanças de fase, é chamada de calor sensível, e pode ser calculado da seguinte maneira:
Q = m cdot c cdot Delta T tag 1
Onde m é a massa, c é o calor específico e Delta T é a variação de temperatura. Assim, vamos analisar cada uma das alternativas:
a) 400 g de água de 20 °C para 70 °C, a água necessitaria receber mais que 8 kcal.
Correta. Substituindo os valores na equação (1), temos:
Q = 400 cancel g cdot 1 dfrac { cal } { cancel g cancel {°C} } cdot (70-20)cancel {°C}
Q = 20.000 , cal
Q = 20 ,kcal
Ou seja, para que se varie a temperatura de 400 g de água de 20 °C para 70 °C, a água necessitaria receber mais de 8 kcal.
b) 1 kg de água em 10 °C, seriam necessárias 1 kcal.
Incorreta. Substituindo os valores na equação (1), temos:
Q = 1000 cancel g cdot 1 dfrac { cal } { cancel g cancel {°C} } cdot 10 cancel {°C}
Q = 10.000 , cal
Q = 10 ,kcal
Logo, seriam necessárias 10 kcal, e não 1 kcal.
c) 10 g de água de 30 °C para 10 °C, a água necessitaria receber 200 cal de calor.
Incorreta. Nesse caso, a água é resfriada em 20 °C (Delta T = 10 - 30 = - 20 °C). Substituindo os valores na equação (1), temos:
Q = 10 cancel g cdot 1 dfrac { cal } { cancel g cancel {°C} } cdot (10-30)cancel {°C}
Q = -200 , cal
Note que, para variar a temperatura da água de 30 °C para 10 °C, a água necessitaria ceder 200 cal de calor, e não receber.
d) 200 g de água de 20 °C para 40 °C, a água necessitaria receber 400 cal de calor.
Incorreta. Substituindo os valores na equação (1), temos:
Q = 200 cancel g cdot 1 dfrac { cal } { cancel g cancel {°C} } cdot (40-20)cancel {°C}
Q = 4.000 , cal
Seriam necessárias 4.000 cal, e não 400 cal.
e) 200 g de água de 50 °C para 10 °C, a água necessitaria ceder menos que 4 kcal de calor.
Incorreta. Substituindo os valores na equação (1), temos:
Q = 200 cancel g cdot 1 dfrac { cal } { cancel g cancel {°C} } cdot (10-50)cancel {°C}
Q = -8.000 , cal
Q = -8 ,kcal
Nesse caso, a água necessitaria ceder 8 kcal, que é mais que 4 kcal de calor.
Portanto, a resposta correta é a alternativa (a).
2149) Considerando-se que o coeficiente de dilatação térmica do latão seja muito superior ao coeficiente de dilatação térmica do vidro comum, é correto afirmar que se um vasilhame de vidro comum com sua tampa feita de latão totalmente rosqueada for
- A) esquentado, a tampa irá crescer um pouco menos que o vidro, ficando assim mais apertado ainda.
- B) resfriado, não haverá nenhuma modificação, pois ao estarem juntos, o vidro e o latão irão variar de forma igual.
- C) esquentado, o vidro e o latão irão aumentar de tamanho de forma igual.
- D) resfriado, a tampa irá crescer um pouco mais que o vasilhame, ficando assim menos apertado ainda.
- E) esquentado, a tampa irá crescer mais que o vidro.
A alternativa correta é letra E) esquentado, a tampa irá crescer mais que o vidro.
Gabarito: LETRA E.
Quando um material é aquecido, suas partículas ganham energia e se movem mais, o que geralmente leva a um aumento no volume do material. Dessa forma, o coeficiente de dilatação térmica é uma medida de quanto o tamanho de um material muda por unidade de mudança na temperatura.
Se o coeficiente de dilatação térmica do latão é muito superior ao do vidro comum, isso significa que, sob a mesma variação de temperatura, o latão irá expandir-se mais do que o vidro. Logo, se um vasilhame de vidro comum com sua tampa feita de latão totalmente rosqueada for esquentado, a tampa de latão irá se expandir mais do que o vasilhame de vidro devido ao seu maior coeficiente de dilatação térmica. Isso pode fazer com que a tampa fique menos ajustada ao vasilhame ou até mais fácil de ser removida, uma vez que a expansão do latão será maior do que a do vidro.
Assim, vamos analisar cada uma das alternativas:
a) esquentado, a tampa irá crescer um pouco menos que o vidro, ficando assim mais apertado ainda.
Incorreta. Como mencionado, o coeficiente de dilatação térmica do latão é muito superior ao do vidro. Dessa forma, quando aquecidos, o latão (tampa) se expandirá mais do que o vidro (vasilhame), e não menos. Logo, a tampa não se tornará mais apertada; ao contrário, ela pode se tornar relativamente mais solta em comparação com sua posição inicial devido à sua maior expansão.
b) resfriado, não haverá nenhuma modificação, pois ao estarem juntos, o vidro e o latão irão variar de forma igual.
Incorreta. Ao serem resfriados, eles não variarão de forma igual. O latão, tendo um coeficiente de dilatação térmica maior, contrairá mais do que o vidro quando ambos forem submetidos a uma diminuição de temperatura.
c) esquentado, o vidro e o latão irão aumentar de tamanho de forma igual.
Incorreta. Como mencionado, o latão se expandirá mais que o vidro para a mesma variação de temperatura devido ao seu maior coeficiente de dilatação térmica.
d) resfriado, a tampa irá crescer um pouco mais que o vasilhame, ficando assim menos apertado ainda.
Incorreta. Ao serem resfriados, tanto o latão quanto o vidro irão contrair (diminuir de tamanho) e não crescer.
e) esquentado, a tampa irá crescer mais que o vidro.
Correta. Considerando que o latão tem um coeficiente de dilatação térmica muito superior ao do vidro. Quando aquecidos, a tampa de latão expandirá mais do que o corpo do vasilhame de vidro, o que pode tornar a tampa menos apertada ou mais fácil de abrir.
Portanto, a resposta correta é a alternativa (e).
2150) Um reservatório de água quente, mantido a uma temperatura de 45 °C, está conectado por um canal subterrâneo a um outro reservatório de água fria, mantido a uma temperatura de 5 °C. Ambos os reservatórios têm superfície livre em contato com ar e estão submetidos a mesma pressão atmosférica.
- A) 1,0034 h.
- B) 1,0009 h.
- C) 1,0013 h.
- D) 1,0052 h.
- E) 1,0065 h.
A alternativa correta é letra D) 1,0052 h.
Notem que no reservatório quente de água, a densidade do líquido rho é menor do que no reservatório frio. Isso porque a maior temperatura do líquido quente expande o volume de água. Lembrando que a densidade é dada por:
rho=frac{m}{V}tag 1
Onde m é a massa do líquido e V é o seu volume. Podemos perceber que para um volume maior teremos uma densidade menor. E qual seria o valor da densidade da água quente em função da densidade da água fria?
Considerando a dilatação de volume da água quente temos que:
V=V_o+V_ocdotgammaDelta{T}
V=V_o+V_ocdot1,3times10^{-4}cdot(45-5)
V=(1+52times10^{-4})V_o=1,0052V_o
Obs: V é o volume da água quente e V_o o volume da água fria.
Logo a densidade da água quente será igual a:
rho=frac{m}{1,0052V_o}
rho=frac{rho_{o}'}{1,0052}
Onde rho_o' é a densidade da água fria. Portanto, utilizando a definição de pressão equivalente à coluna de água para ambos os lados quente e frio teremos :
frac{rho_{o}'}{1,0052}cdot gcdot h_q=rho_o'cdot gcdot h_f
frac{1}{1,0052}cdot h_q=h_f
boxed{h_q=1,0052h_f}
Gabarito: Letra D
