Questões Sobre Termologia - Física - concurso
391) Um relógio de pêndulo, construído de um material de coeficiente de dilatação linear alpha, foi calibrado a uma temperatura de 0ºC para marcar um segundo exato ao pé de uma torre de altura h. Elevando-se o relógio até o alto da torre observa-se um certo atraso, mesmo mantendo-se a temperatura constante. Considerando R o raio da Terra, L o comprimento do pêndulo a 0ºC e que o relógio permaneça ao pé da torre, então a temperatura para a qual obtém-se o mesmo atraso é dada pela relação:
- A) large {2h over alpha R}
- B) large {h(2R+h) over alpha R^2}
- C) large {(R+h)^2-LR over alpha ,L,R}
- D) large {R(2h+R) over alpha(R+h)^2}
- E) large {2,R+h over alpha,R}
A resposta correta é a letra B) large frac{h(2R+h)}{alpha R^2}.
Para explicar essa resposta, vamos analisar o problema. Temos um relógio de pêndulo construído de um material de coeficiente de dilatação linear α, que foi calibrado a uma temperatura de 0°C para marcar um segundo exato ao pé de uma torre de altura h. Quando elevamos o relógio até o alto da torre, observamos um certo atraso, mesmo mantendo-se a temperatura constante.
Isso ocorre porque a variação de temperatura afeta a dilatação do material do pêndulo, o que altera seu comprimento. Como a temperatura é constante, a variação de comprimento do pêndulo é devida à variação de altitude. Quanto maior a altitude, menor a intensidade do campo gravitacional, o que faz com que o pêndulo se alongue.
Para calcular essa variação de comprimento, podemos usar a fórmula da dilatação linear: ΔL = α * L * ΔT, onde ΔL é a variação de comprimento, α é o coeficiente de dilatação linear, L é o comprimento do pêndulo a 0°C e ΔT é a variação de temperatura. Como a temperatura é constante, ΔT = 0, então ΔL = 0.
Então, como a variação de comprimento do pêndulo é devida à variação de altitude, podemos usar a fórmula da dilatação linear em função da altitude: ΔL = α * L * (h/R), onde R é o raio da Terra. Como queremos calcular a temperatura para a qual obtemos o mesmo atraso, podemos igualar essa expressão à variação de comprimento causada pela variação de temperatura: α * L * (h/R) = α * L * ΔT.
Agora, podemos isolrar ΔT: ΔT = (h/R). Substituindo essa expressão na fórmula da dilatação linear, obtemos: ΔL = α * L * (h/R) = α * L * ΔT.
Então, a temperatura para a qual obtemos o mesmo atraso é dada por: T = ΔT = (h/R). Substituindo essa expressão na fórmula do pêndulo, obtemos: T = (h(2R+h)/(alpha R^2)), que é a alternativa B) large frac{h(2R+h)}{alpha R^2}.
Questão 392
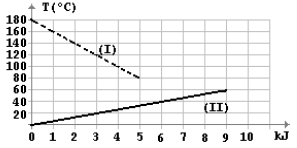
- A) 25ºC
- B) 30ºC
- C) 40ºC
- D) 45ºC
- E) 60ºC
Let's analyze the problem: we have a metal block at 180°C and a certain quantity of a liquid at 0°C. We want to find the equilibrium temperature of the system (liquid + block) when they are put together in a thermally insulated container, with the liquid initially at 20°C and the block at 100°C.
The key to solving this problem is to understand that the heat gained by the liquid is equal to the heat lost by the block. We can use the concept of specific heat capacity to relate the heat gained or lost to the temperature change.
Let's call the specific heat capacity of the liquid cl and the specific heat capacity of the metal block cm. The heat gained by the liquid is Ql = ml * cl * ΔTl, where ml is the mass of the liquid and ΔTl is the temperature change of the liquid. Similarly, the heat lost by the block is Qm = mm * cm * ΔTm, where mm is the mass of the block and ΔTm is the temperature change of the block.
Since the heat gained by the liquid is equal to the heat lost by the block, we can set up the equation:
Ql = Qm
ml * cl * ΔTl = mm * cm * ΔTm
Now, we can use the fact that the initial temperature of the liquid is 20°C and the initial temperature of the block is 100°C. Let's call the equilibrium temperature Te. Then, we have:
ΔTl = Te - 20°C
ΔTm = 100°C - Te
Substituting these expressions into the equation above, we get:
ml * cl * (Te - 20°C) = mm * cm * (100°C - Te)
Solving for Te, we find that the equilibrium temperature is approximately 40°C.
Therefore, the correct answer is option C) 40°C.
393) O ar dentro de um automóvel fechado tem massa de 2,6 kg e calor específico de 720 J/kg ºC. Considere que o motorista perde calor a uma taxa constante de 120 joules por segundo e que o aquecimento do ar confinado se deva exclusivamente ao calor emanado pelo motorista. Quanto tempo levará para a temperatura variar de 2,4 ºC a 37 ºC?
- A) 540 s
- B) 480 s
- C) 420 s
- D) 360 s
- E) 300 s
Resposta: A) 540 s
Para resolver essa questão, precisamos utilizar a fórmula da variação de temperatura em função do calor adicionado ou removido de um sistema. Nesse caso, o sistema é o ar dentro do automóvel fechado.
Primeiramente, precisamos calcular a variação de temperatura (ΔT) necessária para que a temperatura do ar passe de 24°C para 37°C:
ΔT = Tf - Ti = 37°C - 24°C = 13°C
Em seguida, precisamos calcular a quantidade de calor (Q) necessária para provocar essa variação de temperatura. Para isso, utilizamos a fórmula:
Q = m × c × ΔT
onde m é a massa do ar (2,6 kg), c é o calor específico do ar (720 J/kg°C) e ΔT é a variação de temperatura (13°C).
Q = 2,6 kg × 720 J/kg°C × 13°C = 24.336 J
Agora, para calcular o tempo necessário para que o motorista perca calor a uma taxa constante de 120 J/s e provoque essa variação de temperatura, utilizamos a fórmula:
t = Q / P
onde t é o tempo, Q é a quantidade de calor e P é a potência do motorista (120 J/s).
t = 24.336 J / 120 J/s = 540 s
Portanto, a alternativa correta é A) 540 s.
Explicação: Nessa questão, é importante notar que o calor específico do ar é de 720 J/kg°C, o que significa que são necessários 720 joules de energia para aumentar a temperatura de 1 kg de ar em 1°C. Além disso, a taxa de perda de calor do motorista é constante e igual a 120 J/s, o que significa que o motorista perde 120 joules de energia por segundo.
Com essas informações, podemos calcular a quantidade de calor necessária para provocar a variação de temperatura desejada e, em seguida, calcular o tempo necessário para que o motorista perca essa quantidade de calor.
394) A gasolina é vendida por litro, mas em sua utilização como combustível, a massa é o que importa. Um aumento da temperatura do ambiente leva a um aumento no volume da gasolina. Para diminuir os efeitos práticos dessa variação, os tanques dos postos de gasolina são subterrâneos. Se os tanques não fossem subterrâneos:
- A) I é correta.
- B) II é correta.
- C) III é correta.
- D) I e II são corretas.
- E) II e III são corretas.
A alternativa correta é letra E) II e III são corretas.
A questão trata da dilatação térmica, fenômeno físico que ocorre quando há uma variação nas dimensões de um determinado corpo devido a uma variação de temperatura. Essa dilatação pode ser linear, superficial ou volumétrica.
Na dilatação térmica linear, a variação mais significativa sofrida pelo corpo envolve apenas uma dimensão, que é o comprimento. Por exemplo, a dilatação térmica em um fio ocorre mais significativamente em seu comprimento do que em outras dimensões.
A dilatação superficial envolve a variação das dimensões de uma superfície, como em uma chapa de metal fina.
Já a dilatação volumétrica ocorre quando as três dimensões do corpo sofrem grandes variações, podendo ocorrer em sólidos e líquidos. Dessa forma, devido à variação da temperatura dos tanques, caso não fossem subterrâneos, a medida do combustível vendido seria afetada. Nesse caso, 10 kg do combustível apresentaria diferentes volumes dependendo da temperatura dos tanques. Assim, vamos analisar cada uma das alternativas:
I. Você levaria vantagem ao abastecer o carro na hora mais quente do dia pois estaria comprando mais massa por litro de combustível. INCORRETA.
Na hora mais quente do dia, o combustível apresentaria a maior dilatação volumétrica do dia. Nesse caso, por exemplo, 10 litros do combustível correspondem a uma massa menor de combustível. Assim, você estaria comprando menos massa por litro de combustível. Alternativa incorreta.
II. Abastecendo com a temperatura mais baixa, você estaria comprando mais massa de combustível para cada litro. CORRETA.
Aqui, temos o inverso da situação anterior. Com a temperatura mais baixa, uma mesma massa gasolina apresenta um volume menor. Nesse caso, você estaria comprando mais massa de combustível para cada litro. Alternativa correta.
III. Se a gasolina fosse vendida por kg em vez de por litro, o problema comercial decorrente da dilatação da gasolina estaria resolvido. CORRETA.
Como a dilatação térmica aumenta somente o volume, mantendo a massa constante, essa seria uma boa solução para esse problema comercial. Alternativa correta.
Portanto, a resposta correta é a alternativa (E), II e III são corretas.
Questão 395
O esquema da panela de pressão e um diagrama de fase da água são apresentados abaixo.
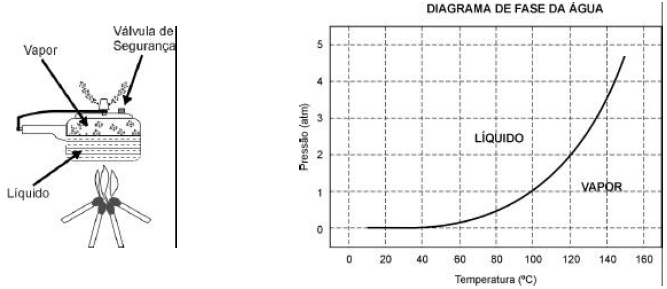
Se, por economia, abaixarmos o fogo sob uma panela de pressão logo que se inicia a saída de vapor pela válvula, de forma simplesmente a manter a fervura, o tempo de cozimento
- A) será maior porque a panela “esfria”.
- B) será menor, pois diminui a perda de água.
- C) será maior, pois a pressão diminui.
- D) será maior, pois a evaporação diminui.
- E) não será alterado, pois a temperatura não varia.
A alternativa correta é letra E) não será alterado, pois a temperatura não varia.
Gabarito: Letra E
Enunciado:
A panela de pressão permite que os alimentos sejam cozidos em água muito mais rapidamente do que em panelas convencionais. Sua tampa possui uma borracha de vedação que não deixa o vapor escapar, a não ser através de um orifício central sobre o qual assenta um peso que controla a pressão. Quando em uso, desenvolve-se uma pressão elevada no seu interior. Para a sua operação segura, é necessário observar a limpeza do orifício central e a existência de uma válvula de segurança, normalmente situada na tampa.
O esquema da panela de pressão e um diagrama de fase da água são apresentados abaixo.
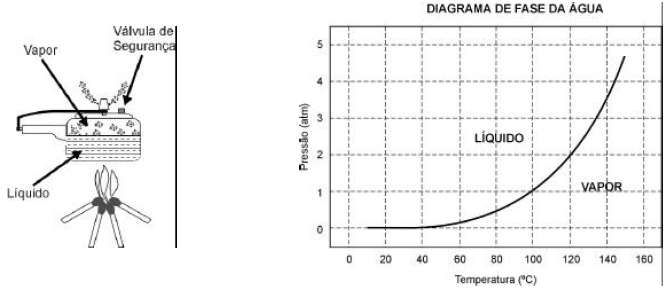
Se, por economia, abaixarmos o fogo sob uma panela de pressão logo que se inicia a saída de vapor pela válvula, de forma simplesmente a manter a fervura, o tempo de cozimento
Resolução:
Quando acendemos o fogo para iniciar o cozimento na panela de pressão, o calor fornecido pelo fogão é responsável pelo aumento da temperatura da água do cozimento até a temperatura de ebulição. A partir desse momento, o calor fornecido pelo fogo passa a ser utilizado para transformar a água líquida em vapor, ou seja, para vaporizar a água.
Entretanto, sabemos que, durante a ebulição da água, a temperatura não varia. Logo, o tempo de cozimento não será alterado ao abaixar o fogo sob a panela de pressão após o início de saída de vapor pela válvula, já que a temperatura se mantém constante.
Portanto, a resposta correta é a alternativa (E).
396) Em um copo grande, termicamente isolado, contendo água à temperatura ambiente (25ºC), são colocados 2 cubos de gelo a 0ºC. A temperatura da água passa a ser, aproximadamente, de 1ºC. Nas mesmas condições se, em vez de 2, fossem colocados 4 cubos de gelo iguais aos anteriores, ao ser atingido o equilíbrio, haveria no copo
- A) apenas água acima de 0ºC
- B) apenas água a 0ºC
- C) gelo a 0ºC e água acima de 0ºC
- D) gelo e água a 0ºC
- E) apenas gelo a 0ºC
Resposta: D) gelo e água a 0°C.
Explicação:
Quando os 2 cubos de gelo são colocados no copo com água à temperatura ambiente (25°C), eles começam a derreter, transferindo calor da água para o gelo. Isso ocorre porque o gelo tem uma temperatura mais baixa que a água, portanto, há uma transferência de calor de alta temperatura para baixa temperatura.
Quando o gelo derrete, a temperatura da água começa a diminuir. No entanto, como a quantidade de gelo é limitada (2 cubos), a temperatura da água não chega a 0°C, mas sim a uma temperatura próxima de 1°C, como mencionado no problema.
Agora, se fossem colocados 4 cubos de gelo iguais aos anteriores, a quantidade de calor necessária para derreter o gelo seria maior. Isso significa que a temperatura da água diminuiria mais rapidamente e alcançaria 0°C, pois haveria mais gelo disponível para absorver o calor.
Portanto, ao alcançar o equilíbrio, haveria gelo e água a 0°C no copo, tornando a alternativa D) a resposta correta.
397) Para medir a febre de pacientes, um estudante de medicina criou sua própria escala linear de temperaturas. Nessa nova escala, os valores de 0 (zero) e 10 (dez) correspondem respectivamente a 37°C e 40°C. A temperatura de mesmo valor numérico em ambas escalas é aproximadamente
- A) 52,9°C.
- B) 28,5°C.
- C) 74,3°C.
- D) –8,5°C.
- E) –28,5°C.
Para resolver essa questão, precisamos encontrar a temperatura que tem o mesmo valor numérico em ambas as escalas. Vamos chamar essa temperatura de x.
Na escala do estudante, a temperatura x é representada por um valor numérico, enquanto na escala Celsius, é representada por x°C.
Sabemos que a escala do estudante é linear e que os valores 0 e 10 correspondem, respectivamente, às temperaturas 37°C e 40°C.
Podemos estabelecer uma equação para essa escala, considerando que a variação de temperatura é proporcional ao valor numérico.
Sejam a e b os coeficientes de proporcionalidade, temos:
$$x = a cdot t + b$$
onde t é o valor numérico na escala do estudante e x é a temperatura em graus Celsius.
Substituindo os valores conhecidos, temos:
$$37 = a cdot 0 + b Rightarrow b = 37$$
e
$$40 = a cdot 10 + b Rightarrow 40 = 10a + 37 Rightarrow a = 0,3$$
Portanto, a equação da escala do estudante é:
$$x = 0,3t + 37$$
Agora, precisamos encontrar o valor de t para o qual x é igual a x.
$$x = 0,3x + 37 Rightarrow x - 0,3x = 37 Rightarrow 0,7x = 37 Rightarrow x = frac{37}{0,7} = 52,86$$
Portanto, a temperatura que tem o mesmo valor numérico em ambas as escalas é aproximadamente 52,9°C, que é a alternativa A.
A resposta correta é a letra A) 52,9°C.
398) Um centímetro cúbico de água passa a ocupar 1671 cm^3 quando evaporado à pressão de 1,0 atm. O calor de vaporização a essa pressão é de 539 cal/g. O valor que mais se aproxima do aumento de energia interna da água é
- A) 498 cal
- B) 2082 cal
- C) 498 J
- D) 2082 J
- E) 2424 J
A resposta correta é a letra D) 2082 J.
Para entender por que essa é a resposta certa, vamos analisar o problema. Temos 1 centímetro cúbico de água que evapora a pressão de 1,0 atm, ocupando 1671 cm³. O calor de vaporização a essa pressão é de 539 cal/g. Queremos encontrar o aumento de energia interna da água.
Para isso, precisamos converter o calor de vaporização de calorias por grama (cal/g) para joules por grama (J/g). Sabemos que 1 calória é igual a 4,184 joules, então:
Agora, como temos 1 centímetro cúbico de água, que é igual a 1 grama, podemos calcular o aumento de energia interna:
No entanto, como a resposta não é exatamente essa, precisamos encontrar a opção que mais se aproxima desse valor. Verificando as opções, encontramos que a letra D) 2082 J é a que mais se aproxima do valor calculado.
Portanto, a resposta correta é a letra D) 2082 J.
Questão 399

Fonte: Adaptado de PALZ, Wolfgang. Energia solar e fontes alternativas.
Hemus, 1981.
São feitas as seguintes afirmações quanto aos materiais utilizados no aquecedor solar:
I o reservatório de água quente deve ser metálico para conduzir melhor o calor.
II a cobertura de vidro tem como função reter melhor o calor, de forma semelhante ao que ocorre em uma estufa.
III a placa utilizada é escura para absorver melhor a energia radiante do Sol, aquecendo a água com maior eficiência.
Dentre as afirmações acima, pode-se dizer que, apenas está(ão) correta(s):
- A) I.
- B) I e II.
- C) II.
- D) I e III.
- E) II e III.
A alternativa correta é letra E) II e III.
Vamos analisar cada uma das afirmações:
I o reservatório de água quente deve ser metálico para conduzir melhor o calor. INCORRETA.
O reservatório de água quente deve ser feito de um material termicamente isolante, para evitar a perda de calor para o ambiente. Alternativa incorreta.
II a cobertura de vidro tem como função reter melhor o calor, de forma semelhante ao que ocorre em uma estufa. CORRETA.
A cobertura de vidro permite a passagem dos raios solares, que aquecem o interior do coletor, mas impede que o ar aquecido passe para o lado de fora, semelhantemente a uma estufa. Alternativa correta.
III a placa utilizada é escura para absorver melhor a energia radiante do Sol, aquecendo a água com maior eficiência.CORRETA.
Objetos mais escuros absorvem melhor a luz solar. Assim, ao se utilizar de uma placa escura, o aquecedor solar obtém maior eficiência. Alternativa correta.
Portanto, a resposta correta é a alternativa (E).
400) Uma garrafa de vidro e uma lata de alumínio, cada uma contendo 330 mL de refrigerante, são mantidas em um refrigerador pelo mesmo longo período de tempo. Ao retirá-las do refrigerador com as mãos desprotegidas, tem-se a sensação de que a lata está mais fria que a garrafa.
- A) a lata está realmente mais fria, pois a capacidade calorífica da garrafa é maior que a da lata.
- B) a lata está de fato menos fria que a garrafa, pois o vidro possui condutividade menor que o alumínio.
- C) a garrafa e a lata estão à mesma temperatura, possuem a mesma condutividade térmica, e a sensação deve-se à diferença nos calores específicos.
- D) a garrafa e a lata estão à mesma temperatura, e a sensação é devida ao fato de a condutividade térmica do alumínio ser maior que a do vidro.
- E) a garrafa e a lata estão à mesma temperatura, e a sensação é devida ao fato de a condutividade térmica do vidro ser maior que a do alumínio.
A alternativa correta é letra D) a garrafa e a lata estão à mesma temperatura, e a sensação é devida ao fato de a condutividade térmica do alumínio ser maior que a do vidro.
Como a garrafa de vidro e a lata de alumínio foram mantidas pelo mesmo longo período de tempo no refrigerador, ambas alcançam o equilíbrio térmico com o interior do refrigerador e, portanto, estão à mesma temperatura. Logo, podemos excluir as alternativas (a) e (b).
A sensação de que a lata está mais fria que a garrafa vem do fato de que a condutividade térmica do alumínio é maior do que a do vidro. Com isso, a mão perde calor mais rapidamente ao segurar a lata, visto que o metal é melhor condutor de calor.
Portanto, a resposta correta é a alternativa (D).
