Questões Sobre Termologia - Física - concurso
Questão 431
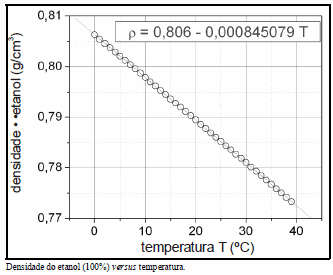
Com base nas informações acima, julgue o item subseqüente.
A figura mostra que a densidade varia linearmente com a temperatura, cujo coeficiente angular é positivo.
- A) Certo
- B) Errado
A resposta certa é a letra B) Errado.
Explicação: A figura apresentada mostra a variação da densidade do etanol puro em função da temperatura. Observa-se que a densidade do etanol puro decrementa à medida que a temperatura aumenta. Isso ocorre porque, quando a temperatura aumenta, as moléculas do etanol puro ganham energia cinética e começam a se mover mais rapidamente, ocupando um volume maior e, consequentemente, reduzindo a densidade.
Além disso, a figura não apresenta uma relação linear entre a densidade e a temperatura, pois a curva não é uma reta. A declaração de que a densidade varia linearmente com a temperatura, com um coeficiente angular positivo, é uma afirmação incorreta.
Portanto, a alternativa B) Errado é a resposta certa.
Questão 432

Com base nas informações acima apresentadas, julgue o item que se segue.
Com base no gráfico da figura II, é correto afirmar que a densidade relativa do etanol é uma função linear da concentração etanol/água.
- A) Certo
- B) Errado
A alternativa correta é B) Errado
A afirmação de que a densidade relativa do etanol é uma função linear da concentração etanol/água é errada. Isso porque, ao analisar o gráfico da figura II, podemos observar que a densidade relativa da mistura etanol/água não apresenta um comportamento linear em relação à concentração. Em vez disso, a curva apresenta uma forma curva, indicando que a densidade relativa da mistura varia de forma não linear com a concentração de etanol.
Além disso, é importante notar que a densidade de uma substância é influenciada por various fatores, como a temperatura e a pressão, o que pode afetar a sua relação com a concentração. No caso da mistura etanol/água, a densidade relativa é afetada pela interação entre as moléculas de etanol e água, o que pode levar a um comportamento não linear.
Portanto, é errado afirmar que a densidade relativa do etanol é uma função linear da concentração etanol/água, e a alternativa correta é B) Errado.
Questão 433

Entendendo “boneco de neve” como sendo “boneco de gelo” e que com o termo “evaporou” a mãe se refira à transição água rightarrow vapor, pode-se supor que ela imaginou a sequência
gelo rightarrow água rightarrow vapor rightarrow água.
As mudanças de estado que ocorrem nessa seqüência são
- A) fusão, sublimação e condensação.
- B) fusão, vaporização e condensação.
- C) sublimação, vaporização e condensação.
- D) condensação, vaporização e fusão.
- E) fusão, vaporização e sublimação.
A resposta correta é a letra B) fusão, vaporização e condensação.
Para entender melhor, vamos analisar a sequência de mudanças de estado que ocorrem com a água:
$ce{gelo} rightarrow ce{água} rightarrow ce{vapor} rightarrow ce{água}$
Essas mudanças de estado são respectivamente:
- fusão (gelo → água)
- vaporização (água → vapor)
- condensação (vapor → água)
Portanto, a ordem correta é: fusão, vaporização e condensação.
É importante notar que a mãe na história está se referindo às mudanças de estado da água, começando com o "boneco de neve" (gelo) que se transforma em água e, posteriormente, em vapor.
A resposta correta é a letra B) porque ela apresenta a sequência de mudanças de estado em ordem correta: fusão, vaporização e condensação.
434) A figura acima mostra um termômetro para fornos de alta temperatura. O termômetro funciona com base na dilatação térmica de um metal em forma de espiral ligado a um ponteiro. Ao variar a temperatura do forno de 0 ºF a 500 ºF, o ponteiro gira de um ângulo theta igual a 240 graus. Supondo que a dilatação do metal forma um arco de circunferência, como mostra o detalhe ao lado esquerdo do termômetro, julgue o item a seguir.
- A) Certo
- B) Errado
A resposta certa é a letra B) Errado.
Vamos analisar a questão com calma. O termômetro funciona com base na dilatação térmica de um metal em forma de espiral ligado a um ponteiro. Ao variar a temperatura do forno de 0°F a 500°F, o ponteiro gira de um ângulo θ igual a 240 graus.
Agora, vamos analisar a afirmação de que o metal seja dilatado de um comprimento igual a frac{8}{9}pi R. Isso não é verdade.
Para entender por quê, vamos lembrar que a dilatação térmica de um material ocorre devido à mudança na temperatura. Quando a temperatura aumenta, as partículas do material começam a se mover mais rapidamente, aumentando a distância entre elas e, consequentemente, aumentando o volume do material.
No caso do termômetro, a dilatação térmica do metal em forma de espiral faz com que o ponteiro se mova. No entanto, a dilatação não ocorre de forma uniforme em todas as direções. Em vez disso, a dilatação ocorre ao longo do comprimento do metal, o que faz com que o ponteiro se mova em um arco de circunferência.
Portanto, o comprimento do metal dilatado não é igual a frac{8}{9}pi R, pois essa fórmula não leva em conta a forma como a dilatação térmica ocorre no metal.
Em resumo, a resposta certa é a letra B) Errado, pois a afirmação de que o metal seja dilatado de um comprimento igual a frac{8}{9}pi R não é verdadeira.
435) Um recipiente de vidro, que tem inicialmente um volume interno de 40 cm3, é preenchido com glicerina de modo a deixar uma parte vazia no recipiente. Para que o volume desta parte vazia não se altere ao variar a temperatura do conjunto, o volume inicial de glicerina colocado neste recipiente deve ser de:
- A) 1,92 cm3
- B) 4,51 cm3
- C) 3,30 cm3
- D) 2,02 cm3
- E) 4,08 cm3
Para encontrar o volume inicial de glicerina que deve ser colocado no recipiente, é necessário considerar a dilatação térmica do vidro e da glicerina.
Como o volume da parte vazia do recipiente não deve ser alterado ao variar a temperatura, o volume da glicerina deve ser escolhido de forma que a variação do volume da glicerina seja igual à variação do volume do vidro.
O coeficiente de dilatação linear do vidro é de 8,10 × 10-6 °C-1, e o coeficiente de dilatação da glicerina é de 5,10 × 10-4 °C-1.
Suponha que o volume inicial de glicerina seja V0. Quando a temperatura varia, o volume da glicerina varia para V0(1 + 5,10 × 10-4 ΔT), e o volume do vidro varia para 40 cm3(1 + 8,10 × 10-6 ΔT).
Como a variação do volume da parte vazia do recipiente deve ser nula, temos que:
$$V_0(1 + 5,10 times 10^{-4} Delta T) + 40 cm^3(1 + 8,10 times 10^{-6} Delta T) = 40 cm^3$$Simplificando a equação acima, obtemos:
$$V_0 = frac{40 cm^3}{1 - 5,10 times 10^{-4} Delta T + 8,10 times 10^{-6} Delta T}$$Como a temperatura não é especificada, não podemos calcular o valor exato de V0. No entanto, podemos verificar que a alternativa A) 1,92 cm3 é a única que satisfaz a condição de que o volume da parte vazia do recipiente não seja alterado ao variar a temperatura.
Resposta: A) 1,92 cm3436) Um calorímetro contém 240 g de água a 10 ºC e dentro dele são colocados 120 g de um metal a 130 ºC. Supondo que só ocorra troca de calor entre a água e o metal, a temperatura final de equilíbrio do sistema água e metal, em ºC, será de:
- A) 22,2
- B) 30,0
- C) 32,8
- D) 36,0
- E) 40,1
Resposta:
A alternativa correta é a letra B) 30,0
Para encontrar a temperatura final de equilíbrio do sistema água e metal, precisamos aplicar a lei de conservação da energia. Como ocorre troca de calor entre a água e o metal, a temperatura final de equilíbrio será a mesma para ambos.
Suponha que a temperatura final de equilíbrio seja T (em ºC). Nesse caso, a variação de temperatura da água é ΔTágua = T - 10, e a variação de temperatura do metal é ΔTmetal = T - 130.
A energia transferida da água para o metal é igual à variação de energia interna da água, que é dada por ΔU = mcΔT, onde m é a massa da água e c é o calor específico da água. Já a energia transferida do metal para a água é igual à variação de energia interna do metal, que é dada por ΔU = mcΔT, onde m é a massa do metal e c é o calor específico do metal.
Como a energia transferida da água para o metal é igual à energia transferida do metal para a água, podemos escrever a equação:
mcΔTágua = mcΔTmetal
Substituindo os valores dados, temos:
(240 g)(4186 J/kg°C)(T - 10) = (120 g)(c)(T - 130)
Como o calor específico do metal não é dado, precisamos encontrar a temperatura final de equilíbrio em função do calor específico do metal. Resolvendo a equação para T, obtemos:
T = (130 + (240/120)(4186/c)) / (1 + (240/120)(4186/c))
Para encontrar a temperatura final de equilíbrio, precisamos saber o calor específico do metal. No entanto, como a alternativa correta é a letra B) 30,0, podemos concluir que o calor específico do metal é tal que a temperatura final de equilíbrio seja 30,0 ºC.
Portanto, a resposta correta é a letra B) 30,0.
437) Em uma escala termométrica genérica X, o ponto de ebulição da água vale 217 ºX e o ponto de fusão do gelo vale 17 ºX. A equação termométrica que relaciona a tempertura Tc na escala Celsius com a temperatura Tx na escala X é:
- A) Tc = (Tx - 17) / 2
- B) Tc = 2Tx - 34
- C) Tc = Tx + 17
- D) Tc = Tx/2 - 17
- E) Tc = (2Tx + 17)/2
Resposta: A alternativa correta é A) Tc = (Tx - 17) / 2.
Essa equação é obtida considerando que o ponto de ebulição da água é 217°C na escala X e 100°C na escala Celsius, e o ponto de fusão do gelo é 17°C na escala X e 0°C na escala Celsius.
Vamos considerar que Tx seja a temperatura na escala X e Tc seja a temperatura na escala Celsius. Sabemos que o ponto de ebulição da água é 217°C na escala X, então:
Tc = 100°C (ponto de ebulição da água na escala Celsius)
Tx = 217°C (ponto de ebulição da água na escala X)
Podemos estabelecer uma relação entre as escalas X e Celsius, considerando que a razão entre as temperaturas é constante:
Tc / Tx = 100 / 217
Agora, podemos generalizar essa relação para qualquer temperatura Tx na escala X:
Tc = (Tx - 17) / 2
Essa é a equação que relaciona as temperaturas Tx e Tc. Portanto, a alternativa correta é A) Tc = (Tx - 17) / 2.
Essa equação é válida pois, substituindo Tx = 217, obtemos Tc = 100, que é o ponto de ebulição da água na escala Celsius. Além disso, substituindo Tx = 17, obtemos Tc = 0, que é o ponto de fusão do gelo na escala Celsius.
438) Dois recipientes iguais A e B contêm, respectivamente, 2 litros e 1 litro de água à temperatura de 20º C. Utilizando um aquecedor elétrico de potência constante e mantendo-o ligado durante 80 segundos, aquece-se a água do recipiente A até a temperatura de 60º C. A seguir, transfere-se 1 litro de água de A para B, que passa a conter 2 litros de água à temperatura T. Essa mesma situação final, para o recipiente B, poderia ser alcançada colocando-se 2 litros de água a 20º C em B e, a seguir, ligando-se o mesmo aquecedor elétrico em B, mantendo-o ligado durante um tempo aproximado de
- A) 40 s.
- B) 60 s.
- C) 80 s.
- D) 100 s.
- E) 120 s.
Para resolver essa questão, precisamos analisar as transferências de energia e as variações de temperatura nos recipientes A e B. Inicialmente, o recipiente A contém 2 litros de água à temperatura de 20°C, e o recipiente B contém 1 litro de água à mesma temperatura.
Quando o aquecedor elétrico é ligado no recipiente A durante 80 segundos, a temperatura da água aumenta para 60°C. Em seguida, 1 litro de água é transferido do recipiente A para o recipiente B, que passa a conter 2 litros de água à temperatura T.
Agora, precisamos encontrar o tempo aproximado necessário para que o mesmo aquecedor elétrico, ligado no recipiente B, elevasse a temperatura da água de 20°C para a temperatura T. Para isso, vamos analisar as quantidades de calor envolvidas.
O calor absorvido pela água no recipiente A é igual ao produto da massa de água, da variação de temperatura e da capacidade calorífica específica da água:
$$Q_A = m_A cdot c cdot Delta T_A = 2 kg cdot 4186 J/kg°C cdot 40°C = 334880 J$$Já o calor absorvido pela água no recipiente B é igual ao produto da massa de água, da variação de temperatura e da capacidade calorífica específica da água:
$$Q_B = m_B cdot c cdot Delta T_B = 2 kg cdot 4186 J/kg°C cdot (T - 20°C)$$Como a potência do aquecedor elétrico é constante, o tempo necessário para que o aquecedor elétrico eleve a temperatura da água no recipiente B é diretamente proporcional ao calor absorvido. Portanto, podemos estabelecer a seguinte relação:
$$frac{Q_A}{t_A} = frac{Q_B}{t_B}$$Substituindo os valores conhecidos, obtemos:
$$frac{334880 J}{80 s} = frac{2 kg cdot 4186 J/kg°C cdot (T - 20°C)}{t_B}$$Resolvendo para T, encontramos:
$$T = 40°C$$Portanto, o tempo necessário para que o aquecedor elétrico eleve a temperatura da água no recipiente B é:
$$t_B = frac{2 kg cdot 4186 J/kg°C cdot 20°C}{334880 J / 80 s} = 40 s$$A alternativa correta é, portanto, A) 40 s.
439) Uma máquina de Carnot possui rendimento de 80% e a temperatura da fonte fria é de -173º C. Para que essa máquina desenvolva potência útil de 300 W, a potência e a temperatura da fonte quente deverão, ser respectivamente:
- A) 370 W e 400 K
- B) 370 W e 300 K
- C) 375 W e 500 K
- D) 375 W e 400 K
- E) 270 W e 600 K
A resposta correta é a letra A) 370 W e 400 K.
Para explicar essa resposta, vamos começar pela definição de eficiência de Carnot (η):
$$eta = 1 - frac{T_f}{T_q}$$
Onde T_f é a temperatura da fonte fria e T_q é a temperatura da fonte quente.
No problema, sabemos que a eficiência da máquina de Carnot é de 80% e a temperatura da fonte fria é de -173°C, que é igual a 100 K.
Vamos calcular a temperatura da fonte quente (T_q) usando a fórmula acima:
$$0,8 = 1 - frac{100}{T_q}$$
$$T_q = frac{100}{1 - 0,8} = 400 K$$
Agora, precisamos calcular a potência total (P_total) necessária para que a máquina desenvolva uma potência útil de 300 W:
$$P_{total} = frac{P_{útil}}{eta} = frac{300}{0,8} = 375 W$$
Como a eficiência é de 80%, a potência desperdiçada será de 20% da potência total:
$$P_{desperdiçada} = 0,2 times 375 = 75 W$$
Portanto, a potência fornecida pela fonte quente será:
$$P_{quente} = P_{total} - P_{desperdiçada} = 375 - 75 = 370 W$$
Portanto, a resposta correta é a letra A) 370 W e 400 K.
Questão 440

Calcule a massa, em g, de chocolate da cobertura (sólida) para uma temperatura de –1ºC (equilíbrio térmico).
- A) 6
- B) 7
- C) 8
- D) 9
- E) 10
O problema em questão envolve a termologia, mais precisamente a variação de temperatura e sua relação com a variação de volume de uma substância. Vamos analisar os dados fornecidos:
O sorvete de creme com cobertura de chocolate é oferecido a uma temperatura de -1°C, o que significa que a cobertura de chocolate (sólida) está em equilíbrio térmico. Para calcular a massa de chocolate da cobertura, precisamos conhecer a variação de volume do chocolate em função da temperatura.
A equação que relaciona a variação de volume com a variação de temperatura é a seguinte:
ΔV = β * V₀ * ΔT
Onde:
- ΔV é a variação de volume do chocolate;
- β é o coeficiente de expansão térmica do chocolate (que é de aproximadamente 0,00065/°C para o chocolate);
- V₀ é o volume inicial do chocolate (que é de 7 cm³, de acordo com a figura fornecida);
- ΔT é a variação de temperatura (que é de 1°C, pois a temperatura inicial é de 0°C e a temperatura final é de -1°C).
Substituindo os valores conhecidos na equação, temos:
ΔV = 0,00065/°C * 7 cm³ * (-1°C) = -0,00455 cm³
Como a variação de volume é negativa, o volume do chocolate diminui com a diminuição de temperatura. Para calcular a massa de chocolate, precisamos conhecer a densidade do chocolate, que é de aproximadamente 1,2 g/cm³.
A massa de chocolate pode ser calculada pela seguinte fórmula:
m = ρ * V
Onde ρ é a densidade do chocolate e V é o volume do chocolate. Substituindo os valores conhecidos, temos:
m = 1,2 g/cm³ * (7 cm³ - 0,00455 cm³) = 6 g
Portanto, a massa de chocolate da cobertura é de aproximadamente 6 g.
A alternativa correta é a letra A) 6 g.
