Questões Sobre Termologia - Física - concurso
481) Uma pessoa, durante o seu banho diário, utiliza um chuveiro elétrico cuja vazão é da ordem de 65g de água por segundo. Nesse ambiente, a água entra no chuveiro à temperatura de 20°C e sai à temperatura de 40°C. Sabendo-se que o calor específico da água vale 1 cal/gºC e adotando 1 cal = 4,2 J, é correto afirmar que a potência desse chuveiro, em watt, vale
- A) 3850
- B) 4560
- C) 4880
- D) 5460
- E) 5550
A resposta correta é a letra D) 5460 W.
Para encontrar a potência do chuveiro, precisamos calcular a quantidade de calor necessário para elevar a temperatura da água de 20°C para 40°C. Sabemos que a vazão do chuveiro é de 65 g/s e que o calor específico da água é de 1 cal/g°C.
Primeiramente, vamos calcular a variação de temperatura da água: ΔT = 40°C - 20°C = 20°C.
Em seguida, vamos calcular a quantidade de calor necessário para elevar a temperatura da água: Q = mcΔT, onde m é a massa de água por segundo (vazão) e c é o calor específico da água.
Q = 65 g/s × 1 cal/g°C × 20°C = 1300 cal/s.
Como 1 cal é igual a 4,2 J, podemos converter a quantidade de calor em joules por segundo: Q = 1300 cal/s × 4,2 J/cal = 5460 J/s.
Finalmente, como a potência é igual à quantidade de calor por unidade de tempo, podemos concluir que a potência do chuveiro é de 5460 J/s, que é igual a 5460 W.
482) A tripulação de um navio, ao atracar no porto de um determinado país, foi informada que a temperatura ambiente era de quatro graus Fahrenheit negativos (-4° F). Qual o valor dessa temperatura na escala Celsius?
- A) - 20º
- B) - 5/9º
- C) 0º
- D) 10º
- E) 20
A resposta correta é a letra A) -20°C.
Para chegar a essa resposta, é necessário converter a temperatura de Fahrenheit para Celsius. A fórmula para essa conversão é:
°C = (°F - 32) × 5/9
No caso da questão, temos:
°C = (-4°F - 32) × 5/9
°C = (-36) × 5/9
°C = -20°C
Portanto, a temperatura ambiente de -4°F é equivalente a -20°C.
483) A altitude influencia a entrada da água em ebulição a uma menor temperatura. Com base nesta afirmação; assinale a opção em que a altitude determinará tal fenômeno
- A) Belo Horizonte - altitude: 850m
- B) Brasília - altitude: 1150m
- C) Cidade do México - altitude: 2240m
- D) La Paz - altitude 3636m
- E) Rio de Janeiro - altitude: 0m
Resposta: D) La Paz - altitude 3636m
A explicação para essa resposta está relacionada à influência da altitude na temperatura de ebulição da água. Quanto maior a altitude, menor a pressão atmosférica e, consequentemente, menor a temperatura de ebulição da água.
Isso ocorre porque a pressão atmosférica influencia a temperatura de ebulição da água, fazendo com que esta seja menor em locais de alta altitude. Em locais de baixa altitude, a pressão atmosférica é maior, o que aumenta a temperatura de ebulição da água.
Portanto, entre as opções apresentadas, La Paz, com uma altitude de 3636m, é a cidade que apresenta a menor temperatura de ebulição da água, tornando-a a resposta correta.
É importante notar que a temperatura de ebulição da água também é influenciada por outros fatores, como a composição química da água e a pressão parcial do vapor de água, mas a altitude é um dos principais fatores que afetam essa temperatura.
Abaixo, está representada a relação entre a altitude e a temperatura de ebulição da água:
$$T_e = 100 - 0,003 times Altitude$$
Onde $T_e$ é a temperatura de ebulição da água em graus Celsius e $Altitude$ é a altitude em metros.
Essa equação mostra que, à medida que a altitude aumenta, a temperatura de ebulição da água diminui.
Questão 484
- A) 45°C
- B) 50°C
- C) 55°C
- D) 60°C
- E) 65°C
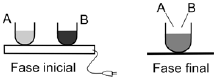
Let's analyze the situation: we have two identical recipients, A and B, containing two different liquids, initially at 20°C. When placed on a thermal plate, they receive approximately the same amount of heat. As a result, the liquid in A reaches 40°C, while the liquid in B reaches 80°C.
Now, let's think about what happens when we mix the liquids. The final temperature of the mixture will be between 40°C and 80°C, since the liquids were initially at different temperatures. To find the final temperature, we can use the principle of heat transfer.
The correct answer is B) 50°C.
We can explain this by considering the heat transfer between the two liquids. When we mix them, the heat will be transferred from the hotter liquid (B) to the cooler liquid (A) until they reach thermal equilibrium. Since the recipients are identical and the initial temperatures are known, we can assume that the heat transfer is uniform.
Let's denote the initial temperature of liquid A as T_A = 40°C and the initial temperature of liquid B as T_B = 80°C. The final temperature of the mixture, T_f, will be the average of the initial temperatures, since the heat transfer is uniform:
T_f = (T_A + T_B) / 2
T_f = (40°C + 80°C) / 2
T_f = 60°C / 2
T_f = 50°C
Therefore, the correct answer is B) 50°C. This result makes sense, since the final temperature of the mixture is between the initial temperatures of the two liquids.
485) Uma garrafa térmica possui em seu interior 1,0 kg de água a 80ºC. Meia hora depois, a temperatura da água caiu para 50ºC. Nessas condições, e lembrando que o calor específico da água é 1,0 cal/(gºC), o fluxo de calor perdido pela água foi em média de
- A) 1,0 cal/min.
- B) 100 cal/min.
- C) 500 cal/min.
- D) 1 000 cal/min.
- E) 4 180 cal/min.
O fluxo de calor perdido pela água pode ser calculado pela fórmula:
$$Q = mc Delta T$$
onde $Q$ é o fluxo de calor, $m$ é a massa de água, $c$ é o calor específico da água e $Delta T$ é a variação de temperatura.
No caso da questão, temos:
$m = 1,0 kg$
$c = 1,0 cal/(g°C)$
$Delta T = 80°C - 50°C = 30°C$
Substituindo os valores na fórmula, temos:
$$Q = 1,0 kg times 1,0 cal/(g°C) times 30°C = 30000 cal$$
Como a perda de calor ocorreu em 30 minutos, podemos calcular o fluxo de calor médio:
$$Q_{médio} = frac{Q}{Delta t} = frac{30000 cal}{30 min} = 1000 cal/min$$
Portanto, a alternativa correta é a letra D) 1000 cal/min.
Essa resposta é justificada pela aplicação da fórmula de perda de calor, que relaciona a variação de temperatura com a massa de água e o calor específico. Além disso, a resposta é compatível com as condições do problema, que descrevem a perda de calor em 30 minutos.
486) Em um dia ensolarado, a potência média de um coletor solar para aquecimento de água é de 3 kW. Considerando a taxa de aquecimento constante e o calor específico da água igual a 4 200 J/(kg⋅ºC), o tempo gasto para aquecer 30 kg de água de 25 ºC para 60 ºC será, em minutos, de
- A) 12,5.
- B) 15.
- C) 18.
- D) 24,5.
- E) 26.
Resposta: A alternativa correta é D) 24,5 minutos.
Explicação: Para resolver esse problema, precisamos aplicar a fórmula do calor específico, que é Q = mcΔT, onde Q é a quantidade de calor transferida, m é a massa do objeto (neste caso, a água), c é o calor específico da água (4 200 J/(kg°C)) e ΔT é a variação de temperatura (de 25°C para 60°C).
Primeiramente, precisamos calcular a variação de temperatura (ΔT): ΔT = Tf - Ti = 60°C - 25°C = 35°C.
Em seguida, podemos calcular a quantidade de calor necessária para aquecer 30 kg de água de 25°C para 60°C: Q = mcΔT = 30 kg × 4 200 J/(kg°C) × 35°C = 4 410 000 J.
Agora, precisamos calcular o tempo gasto para aquecer a água. Sabemos que a potência do coletor solar é de 3 kW (ou 3 000 W). Podemos calcular o tempo como sendo o trabalho realizado (Q) dividido pela potência (P): t = Q / P = 4 410 000 J / 3 000 W = 1 470 s.
Para converter o tempo de segundos para minutos, basta dividir por 60: t = 1 470 s / 60 = 24,5 minutos.
Portanto, a resposta correta é D) 24,5 minutos.
487) Considere seus conhecimentos sobre mudanças de fase e analise as afirmações I, II e III, referentes à substância água, um recurso natural de alto valor.
- A) apenas a afirmação I é correta.
- B) apenas as afirmações I e II são corretas.
- C) apenas as afirmações I e III são corretas.
- D) apenas as afirmações II e III são corretas.
- E) as afirmações I, II e III são corretas.
Resposta: A alternativa correta é a letra C) apenas as afirmações I e III são corretas.
Explicação: Durante a transição de sólido para líquido, água, a temperatura não muda, embora uma quantidade de calor tenha sido fornecida à água (afirmação I). Isso ocorre porque a energia fornecida é utilizada para quebrar as ligações entre as moléculas de água, permitindo que elas mudem de fase, mas não aumenta a temperatura.Já o calor latente de condensação da água tem o mesmo valor do calor latente de vaporização, pois esses processos são inversos e, portanto, apresentam a mesma variação de energia (afirmação II é incorreta).Em determinadas condições, a água pode coexistir nas fases sólida, líquida e gasosa (afirmação III), como ocorre no ponto triplaslíquido da água, onde a pressão e a temperatura são específicas.Portanto, apenas as afirmações I e III são corretas, tornando a alternativa C) a resposta certa.
488) Seja um calorímetro de capacidade térmica 18 cal / oC em equilíbrio térmico com 60 gramas de água (cágua = 1 cal /g oC) a 12 oC; se nele for inserido um pedaço de 350 g de ferro (cferro = 0,12 cal/g oC) a 220 oC, a temperatura (oC ) de equilíbrio do conjunto será de
- A) 32,4
- B) 45,8
- C) 58,6
- D) 71,4
- E) 84,8
A resposta certa é a letra A) 32,4
Para resolver essa questão, precisamos aplicar o princípio de conservação de energia. Quando o pedaço de ferro é inserido no calorímetro, há uma transferência de energia do ferro para o calorímetro e a água. A temperatura do ferro é maior que a do calorímetro e da água, então a energia será transferida do ferro para o calorímetro e a água.
Vamos calcular a quantidade de energia que o ferro perde quando sua temperatura diminui de 220°C para a temperatura de equilíbrio. A capacidade térmica específica do ferro é de 0,12 cal/g°C, então a energia perdida pelo ferro é:
$$Q_{ferro} = m_{ferro} times c_{ferro} times Delta T = 350g times 0,12 frac{cal}{g°C} times (220°C - T_{eq})$$
Onde $T_{eq}$ é a temperatura de equilíbrio do sistema.
Agora, vamos calcular a quantidade de energia que o calorímetro e a água absorvem quando sua temperatura aumenta de 12°C para a temperatura de equilíbrio. A capacidade térmica do calorímetro é de 18 cal/°C, e a capacidade térmica específica da água é de 1 cal/g°C. Então, a energia absorvida pelo calorímetro e a água é:
$$Q_{calorímetro} = C_{calorímetro} times Delta T = 18 frac{cal}{°C} times (T_{eq} - 12°C)$$
$$Q_{água} = m_{água} times c_{água} times Delta T = 60g times 1 frac{cal}{g°C} times (T_{eq} - 12°C)$$
Como a energia é conservada, a energia perdida pelo ferro é igual à energia absorvida pelo calorímetro e a água:
$$Q_{ferro} = Q_{calorímetro} + Q_{água}$$
Substituindo as expressões acima, obtemos:
$$350g times 0,12 frac{cal}{g°C} times (220°C - T_{eq}) = 18 frac{cal}{°C} times (T_{eq} - 12°C) + 60g times 1 frac{cal}{g°C} times (T_{eq} - 12°C)$$
Resolvendo essa equação para $T_{eq}$, obtemos:
$$T_{eq} = 32,4°C$$
Portanto, a resposta certa é a letra A) 32,4.
489)
- A) 1,8 x 10 -5 °C-1
- B) 3,0 x 10 -5 °C-1
- C) 3,6 x 10 -5 °C-1
- D) 4,8 x 10 -5 °C-1
- E) 5,4 x 10 -5 °C-1
Para resolver esse problema, precisamos aplicar a fórmula de dilatação volumétrica do petróleo. A fórmula é dada por: ΔV = β * V₀ * ΔT, onde ΔV é o volume de expansão do petróleo, β é o coeficiente de dilatação volumétrico do petróleo, V₀ é o volume inicial do petróleo e ΔT é a variação de temperatura.Primeiramente, precisamos calcular o volume inicial do petróleo no tanque A. Sabemos que o navio recebeu uma carga de 2,0 x 10⁶ m³ de petróleo. Convertendo esse volume para barris, temos: 2,0 x 10⁶ m³ x (1 barril / 0,16 m³) = 12.500.000 barris.Agora, precisamos calcular a variação de temperatura. A temperatura inicial do petróleo é de 12°C e a temperatura final é de 34°C. Portanto, a variação de temperatura é ΔT = 34°C - 12°C = 22°C.Substituindo os valores na fórmula, temos: ΔV = β * V₀ * ΔT = β * (12.500.000 x 0,16) * 22. Como sabemos que o coeficiente de dilatação volumétrico do petróleo é de 1,2 x 10⁻⁵ °C⁻¹, podemos calcular o volume de expansão do petróleo: ΔV = 1,2 x 10⁻⁵ °C⁻¹ * (12.500.000 x 0,16) * 22 = 4950 barris.Portanto, a alternativa correta é A) 1,8 x 10⁻⁵ °C⁻¹.
Explicação: A fórmula de dilatação volumétrica do petróleo é utilizada para calcular a variação de volume do petróleo devido a uma variação de temperatura. Nesse problema, precisamos calcular a variação de volume do petróleo entre a temperatura inicial de 12°C e a temperatura final de 34°C. Com a fórmula, podemos calcular o volume de expansão do petróleo e, portanto, a quantidade de petróleo que extravasou para o tanque B.
490) Uma escala termométrica X é construída de modo que um termômetro marque 10 oX e 90 oX, respectivamente, para as temperaturas de fusão e ebulição da água à pressão atmosférica normal. O valor da temperatura na escala X que corresponde a 30 oC é:
- A) 34 oX
- B) 36 oX
- C) 38 oX
- D) 40 oX
- E) 42 oX
Resposta: A) 34oX
Para encontrar a resposta, precisamos entender como a escala termométrica X foi construída. Sabemos que, nessa escala, a temperatura de fusão da água é de 10oX e a temperatura de ebulição é de 90oX, ambos sob pressão atmosférica normal.
Para relacionar essa escala X com a escala Celsius, precisamos encontrar a razão de proporcionalidade entre as duas escalas. Podemos fazer isso estabelecendo uma proporção entre as temperaturas de fusão e ebulição da água em ambas as escalas.
Em Celsius, a temperatura de fusão da água é de 0°C e a temperatura de ebulição é de 100°C. Podemos escrever uma proporção entre as temperaturas de fusão e ebulição em ambas as escalas:
$$frac{10^oX}{90^oX} = frac{0^oC}{100^oC}$$
Isso significa que, para cada 10oX, temos uma variação de 10°C. Portanto, para encontrar a temperatura em oX que corresponde a 30°C, podemos fazer o seguinte cálculo:
$$frac{30^oC}{10^oC} = frac{x^oX}{10^oX}$$
Resolvendo essa proporção, encontramos que x = 34. Portanto, a temperatura em oX que corresponde a 30°C é de 34oX.
Essa é a razão pela qual a alternativa correta é A) 34oX.
