Questões Sobre Termologia - Física - concurso
501) Um gás ideal é mantido a temperatura constante. Se reduzirmos seu volume de 20%, de quanto aumentará sua pressão?
- A) 5%
- B) 10%
- C) 15%
- D) 20%
- E) 25%
Para resolver essa questão, precisamos utilizar a equação de estado dos gases ideais, que relaciona a pressão (P), volume (V) e temperatura (T) de um gás ideal:
$$PV = nRT$$
Onde n é a quantidade de matéria do gás e R é a constante dos gases ideais.
Como a temperatura é constante, podemos rearranjar a equação para isolar a pressão:
$$P = frac{nRT}{V}$$
Agora, suponha que o volume inicial seja V0 e a pressão inicial seja P0. Se reduzirmos o volume em 20%, o novo volume será:
$$V = V_0 - 0,2V_0 = 0,8V_0$$
Como a temperatura é constante, a quantidade de matéria também é constante. Portanto, podemos utilizar a equação anterior para encontrar a nova pressão:
$$P = frac{nRT}{0,8V_0} = frac{P_0}{0,8} = 1,25P_0$$
Isso significa que a pressão aumentará em 25%.
A alternativa correta é a letra E) 25%
Essa questão ilustra a relação entre a pressão e o volume de um gás ideal, demonstrando que, à medida que o volume diminui, a pressão aumenta.
502) Em uma planta industrial encontra-se uma parede composta de dois materiais A e B. A parede A, que possui 100 mm de espessura, tem sua extremidade esquerda encontra-se idealmente isolada e apresenta uma geração interna de energia igual a 2 times 10^6 dfrac {W} {m^3}. A parede B possui 20 mm de espessura e sua extremidade livre está sujeita ao ar ambiente, cuja temperatura e coeficiente de filme valem, respectivamente, 30 oC e 1000 dfrac {W} {m^2 ºC}.
- A) 150
- B) 190
- C) 200
- D) 220
- E) 250
A resposta correta para essa questão é a letra E) 250°C.
Para explicar essa resposta, vamos analisar a situação descrita na questão. Temos uma parede composta por dois materiais, A e B. A parede A tem 100 mm de espessura e sua extremidade esquerda está idealmente isolada, apresentando uma geração interna de energia igual a 2 × 10^6 W/m³. Já a parede B tem 20 mm de espessura e sua extremidade livre está sujeita ao ar ambiente, cuja temperatura é de 30°C e coeficiente de filme é de 1000 W/m²°C.
Podemos começar calculando a temperatura na interface entre os materiais A e B. Para isso, podemos utilizar a equação de Fourier para a condução de calor:
$$vec{q} = -k nabla T$$Onde $vec{q}$ é o fluxo de calor, $k$ é a condutividade térmica e $nabla T$ é o gradiente de temperatura. Como a condutividade térmica do material B é igual a 200 W/m°C, podemos calcular a temperatura na interface:
$$T_i = frac{T_A + T_B}{2} + frac{k_B}{h_B} (T_B - T_i)$$Onde $T_i$ é a temperatura na interface, $T_A$ é a temperatura na parede A, $T_B$ é a temperatura na parede B, $k_B$ é a condutividade térmica do material B e $h_B$ é o coeficiente de filme do material B.
Substituindo os valores dados, temos:
$$T_i = frac{T_A + 30}{2} + frac{200}{1000} (30 - T_i)$$Agora, precisamos encontrar a temperatura na parede A. Como a extremidade esquerda da parede A está idealmente isolada, podemos considerar que a temperatura é constante ao longo da parede. Além disso, como há uma geração interna de energia, podemos utilizar a equação de Poisson para a distribuição de temperatura:
$$nabla^2 T = - frac{g}{k}$$Onde $g$ é a geração interna de energia e $k$ é a condutividade térmica. Como a geração interna de energia é igual a 2 × 10^6 W/m³, podemos calcular a temperatura na parede A:
$$T_A = frac{2 times 10^6}{200} + T_i$$Agora, podemos substituir o valor de $T_A$ na equação anterior para encontrar a temperatura na interface:
$$T_i = frac{frac{2 times 10^6}{200} + T_i + 30}{2} + frac{200}{1000} (30 - T_i)$$Resolvendo essa equação, encontramos que a temperatura na interface é igual a 250°C, que é a resposta correta.
Portanto, a temperatura na interface entre os materiais A e B é de 250°C.
Questão 503
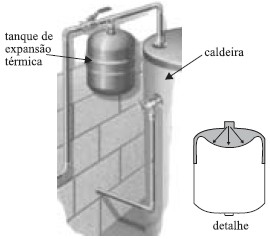
Suponha que você queira proteger uma caldeira de volume 500 L, destinada a aquecer a água de 20 ºC a 80 ºC; que, entre essas temperaturas, pode-se adotar para o coeficiente de dilatação volumétrica da água o valor médio de 4,4 cdot 10–4 ºC–1 e considere desprezíveis a dilatação da caldeira e do tanque. Sabendo que o preço de um tanque de expansão térmica para essa finalidade é diretamente proporcional ao seu volume, assinale, das opções fornecidas, qual deve ser o volume do tanque que pode proporcionar a melhor relação custo-benefício.
- A) 4,0 L.
- B) 8,0 L.
- C) 12 L.
- D) 16 L.
- E) 20 L.
Resposta: A alternativa correta é D) 16 L.
Explicação:
Para calcular o volume do tanque de expansão térmica necessário, precisamos considerar a expansão volumétrica da água entre as temperaturas de 20°C e 80°C. Sabemos que o coeficiente de dilatação volumétrica da água é de 4,4 × 10-4 °C-1.
Primeiramente, vamos calcular a variação de volume da água:
$$Delta V = V_{0} times beta times Delta T$$Onde $V_{0}$ é o volume inicial da água (500 L), $beta$ é o coeficiente de dilatação volumétrica e $Delta T$ é a variação de temperatura (80°C - 20°C = 60°C).
$$Delta V = 500 times 4,4 times 10^{-4} times 60 = 13,2 L$$O volume do tanque de expansão térmica deve ser capaz de acomodar essa variação de volume. Portanto, o volume do tanque deve ser de pelo menos 13,2 L.
Entre as opções fornecidas, a que melhor se aproxima desse valor é a opção D) 16 L.
É importante notar que o volume do tanque de expansão térmica deve ser maior que a variação de volume da água para garantir que a pressão não aumente excessivamente e cause danos à caldeira ou ao tanque.
504) Um estudante contou ao seu professor de Física que colocou uma garrafa PET vazia, fechada, no freezer de sua casa. Depois de algum tempo, abriu o freezer e verificou que a garrafa estava amassada. Na primeira versão do estudante, o volume teria se reduzido de apenas 10% do volume inicial; em uma segunda versão, a redução do volume teria sido bem maior, de 50%. Para avaliar a veracidade dessa história, o professor aplicou à situação descrita a Lei Geral dos Gases Perfeitos, fazendo as seguintes hipóteses, que admitiu verdadeiras:
- A) falou a verdade na primeira versão, pois só essa redução do volume é compatível com a condição de que a pressão interna do freezer seja menor do que a pressão ambiente.
- B) falou a verdade na segunda versão, pois só essa redução do volume é compatível com a condição de que a pressão interna do freezer seja menor do que a pressão ambiente.
- C) mentiu nas duas versões, pois ambas implicariam em uma pressão interna do freezer maior do que a pressão ambiente.
- D) mentiu nas duas versões, pois é impossível a diminuição do volume da garrafa, qualquer que seja a relação entre a pressão interna do freezer e a pressão ambiente.
- E) mentiu nas duas versões, pois nessas condições a garrafa teria estufado ou até mesmo explodido, tendo em vista que a pressão interna do freezer é muito menor do que a pressão ambiente.
A alternativa correta é a letra A) falou a verdade na primeira versão,. pois só essa redução do volume é compatível com a condição de que a pressão interna do freezer seja menor do que a pressão ambiente.
Para entender melhor, vamos analisar a situação. O estudante colocou uma garrafa PET vazia, fechada, no freezer de sua casa. Depois de algum tempo, abriu o freezer e verificou que a garrafa estava amassada. Isso significa que houve uma redução no volume da garrafa.
A Lei Geral dos Gases Perfeitos pode ser aplicada nessa situação. Segundo essa lei, a pressão exercida por um gás é diretamente proporcional à temperatura e inversamente proporcional ao volume. Matematicamente, isso pode ser representado pela fórmula:
$$P_1V_1 = P_2V_2$$
Onde $P_1$ e $V_1$ são a pressão e o volume iniciais, e $P_2$ e $V_2$ são a pressão e o volume finais.
No caso da garrafa no freezer, a temperatura ambiente é de 27°C, e a temperatura do freezer é de -18°C. Isso significa que a temperatura no freezer é muito menor do que a temperatura ambiente. Além disso, o professor assume que houve tempo suficiente para o equilíbrio térmico.
Como a pressão interna do freezer é menor do que a pressão ambiente, a pressão exercida sobre a garrafa é menor do que a pressão ambiente. Segundo a Lei Geral dos Gases Perfeitos, isso significa que o volume da garrafa deve diminuir.
A redução de 10% no volume da garrafa, como relatado na primeira versão do estudante, é compatível com a condição de que a pressão interna do freezer seja menor do que a pressão ambiente. Já a redução de 50% no volume da garrafa, como relatado na segunda versão, não é compatível com essa condição.
Portanto, a resposta correta é a letra A) falou a verdade na primeira versão, pois apenas essa redução do volume é compatível com a condição de que a pressão interna do freezer seja menor do que a pressão ambiente.
Questão 505
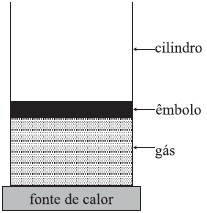
Considere duas situações:
I. o êmbolo pode mover-se livremente, permitindo que o gás se expanda à pressão constante;
II. o êmbolo é fixo, mantendo o gás a volume constante.
Suponha que nas duas situações a mesma quantidade de calor é fornecida a esse gás, por meio dessa fonte. Pode-se afirmar que a temperatura desse gás vai aumentar
- A) igualmente em ambas as situações.
- B) mais em I do que em II.
- C) mais em II do que em I.
- D) em I, mas se mantém constante em II.
- E) em II, mas se mantém constante em I.
Para responder essa questão, devemos primeiro entender como o calor afeta o gás em cada situação.
No caso I, o êmbolo pode se mover livremente, permitindo que o gás se expanda à pressão constante. Isso significa que o gás está fazendo trabalho para se expandir, o que remove energia do gás. Como a mesma quantidade de calor é fornecida em ambas as situações, a temperatura do gás aumentará, mas menos do que na situação II, pois parte da energia é gasta para fazer trabalho.
No caso II, o êmbolo é fixo, mantendo o volume do gás constante. Isso significa que o gás não pode se expandir e, portanto, não faz trabalho. Como resultado, toda a energia do calor fornecido é usada para aumentar a temperatura do gás.
Portanto, podemos concluir que a temperatura do gás aumentará mais na situação II do que na situação I, pois na situação II toda a energia do calor é usada para aumentar a temperatura, enquanto na situação I parte da energia é gasta para fazer trabalho.
A alternativa correta é, portanto, C) mais em II do que em I.
Essa resposta faz sentido, pois a expansão do gás à pressão constante (situação I) remove energia do gás, enquanto a manutenção do volume constante (situação II) permite que toda a energia do calor seja usada para aumentar a temperatura.
506) Um aquecedor, ligado a uma ddp constante de 21 V, sendo percorrido por uma corrente de intensidade 3 A, é utilizado para aquecer 100g de água durante 1 minuto. Qual a temperatura final, sabendo-se que a água está inicialmente a 30° C?
- A) 45° C
- B) 58° C
- C) 27° C
- D) 36° C
- E) 39° C
A alternativa correta é letra E) 39° C
A potência dissipada por efeito joule é dada por:
P = Vcdot i
P = 21 cdot 3
P = 63 J/s
Para calcular a energia que foi dissipada, basta multiplicar a potência pelo tempo. Logo:
E = P cdot t
E = 63 cdot 60
E = 3780 J
Vamos converter essa energia para calorias dividindo a energia em joules por 4,2 conforme os dados do enunciado.
E = frac{3780}{4,2}
E = 900 cal
Essa energia será usada para aquecer a água. Sendo assim.
900 = m cdot c cdot (t_f - t_i)
Onde:
- m é a massa de água em kg
- c é o calor específico da água
- tf é a temperatura final
- ti é a temperatura inicial
900 = 100 cdot 1 cdot (t_f - t_i)
t_f - t_i = 9
t_f = 39
A temperatura final é de 39 graus celsius.
507) área total da parede de um refrigerador doméstico é cerca de 4 m2, e a espessura no isolamento de poliestireno nas paredes é cerca de 20 mm. Supondo que a diferença de temperatura entre o interior e o exterior do refrigerador seja de 20°C, quanto calor flui através dessas paredes no intervalo de 1 hora?
- A) 144 kJ
- B) 100 kJ
- C) 120 kJ
- D) 90 kJ
- E) 85 kJ
A alternativa correta é letra A) 144 kJ
A equação do fluxo de calor é dada por:
Fluxo = frac{k . A . Delta T}{e}
sendo k a condutividade térmica, A a superfície de contato, e a espessura do contato e Delta T a diferença de temperatura entre os meios.
O enunciado nos informou todos esses dados:
k = 0,01 w/m.K
A = 4 m^2
e = 20 mm
Delta T = 20^o C
Para facilitar o uso da equação, levamos todas as medidas ao sistema internacional (S.I.).
Notemos que a área e a constante já estão no S.I. Além disso, a variação de 20^o C corresponde a variação da medida em Kelvin 20 K. Alteramos somente a medida de espessura
e = 20 mm = 20 . 10^{-3} m
Como agora todos os valores estão no S.I., fazemos:
Fluxo = frac{k . A . Delta T}{e}
Fluxo = frac{0,01 . 4 . 20}{20 . 10^{-3}}
Fluxo = frac{0,01 . 4 }{10^{-3}}
Fluxo = 4 . 0,01 10^3 w
Fluxo = 40 w
Sabemos que uma hora corresponde a 3600 segundos:
1 h = 3600 s
Logo,
Calor = Fluxo . Tempo
Calor = 40 . 3600
Calor = 144 . 10^3 J
Como 10^3 corresponde ao prefixo Kilo:
calor = 144 kJ
como indicado na alternativa A.
508) 300 gramas de gelo 0^circ C a foram adicionados a 400 gramas de água a 55^circ C. Assinale a opção CORRETA para a temperatura final do sistema em condição adiabática.
- A) 4− ºC
- B) 3 − ºC
- C) 0 ºC
- D) + 3 ºC
- E) + 4 ºC
Resposta: C) 0°C
Para resolver esse problema, precisamos considerar as seguintes etapas:
1. O gelo a 0°C é adicionado à água a 55°C. Isso significa que o gelo começará a derreter, absorvendo calor da água.
2. A quantidade de calor necessária para derreter 300 g de gelo é igual ao produto da massa do gelo pela sua calor de fusão: Q = m * L = 300 g * 80 cal/g = 24000 cal.
3. Além disso, o gelo também absorverá calor da água para aumentar sua temperatura de 0°C para a temperatura final do sistema. A quantidade de calor necessária para isso é igual ao produto da massa do gelo pela sua calor específico e pela variação de temperatura: Q = m * c * ΔT = 300 g * 0,50 cal/g°C * (Tf - 0°C), onde Tf é a temperatura final do sistema.
4. A água a 55°C transfere calor para o gelo. A quantidade de calor transferida é igual ao produto da massa da água pela sua calor específico e pela variação de temperatura: Q = m * c * ΔT = 400 g * 1 cal/g°C * (55°C - Tf).
5. Como o processo ocorre em condições adiabáticas, a soma das quantidades de calor absorvidas pelo gelo e pela água é igual a zero: Q1 + Q2 + Q3 = 0.
Substituindo as expressões acima, obtemos a equação: 24000 cal + 300 g * 0,50 cal/g°C * (Tf - 0°C) + 400 g * 1 cal/g°C * (55°C - Tf) = 0.
Resolvendo essa equação, encontramos que a temperatura final do sistema é Tf = 0°C.
Portanto, a alternativa correta é C) 0°C.
Explicação:
O processo de derretimento do gelo ocorre à temperatura constante de 0°C, pois o gelo absorve calor da água para derreter. Após o derretimento, o sistema atinge o equilíbrio térmico, e a temperatura final é igual a 0°C.
509) Uma determinada civilização antiga estabeleceu como referência para medição da temperatura uma escala termométrica gamma (gama), tomando como pontos fixos os valores 10°γ para a solidificação da água e 140°γ para evaporação da água. Estabelecendo a relação entre as escalas °gamma (gama) e °C (Celsius), pode-se afirmar que 60°γ corresponde aproximadamente na escala Celsius a:
- A) 75,0
- B) 65,0
- C) 47,5
- D) 38,5
- E) 33,3
A alternativa correta é letra D) 38,5
Para encontrar a relação correta entre as escalas termométricas, é preciso conhecer pelo menos 2 pontos em comum e estabelecer uma relação de proporcionalidade entre os segmentos das escalas. A figura abaixo traz uma relação entre a escala gamma e a escala Celsius para pontos como o ponto de fusão e de ebulição da água ao nível do mar:
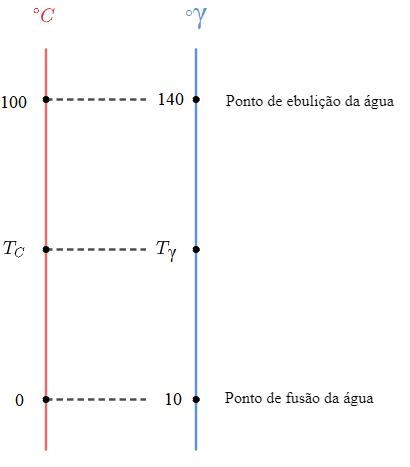
Então, utilizando-se a proporção entre as escalas, temos que:
dfrac { T_C - 0 } { 100 - 0 } = dfrac { T_{gamma} - 10 } { 140 - 10 }
dfrac { T_C } { 100 } = dfrac { T_{gamma} - 10 } { 130 }
Assim, para T_{gamma} = 60° gamma, temos que:
dfrac { T_C } { 100 } = dfrac { 60 - 10 } { 130 }
dfrac { T_C } { 100 } = dfrac { 50 } { 130 }
T_C = dfrac { 100 cdot 50 } { 130 }
T_C approx 38,5 °C
Portanto, a resposta correta é a alternativa (D).
510) Uma barra metálica sofre um aumento linear de 0,15% quando ocorre uma variação de temperatura de 50°C. Deste modo, pode-se concluir que o coeficiente de dilatação linear, em graus recíprocos, deste metal é de:
- A) 3 x 10-5
- B) 3 x 10-4
- C) 3 x 10-3
- D) 3 x 10-2
- E) 3 x 10-1
A alternativa correta é letra A) 3 x 10-5
A dilatação térmica é um fenômeno físico que ocorre quando há uma variação nas dimensões de um determinado corpo devido a uma variação de temperatura. Essa dilatação pode ser linear, superficial ou volumétrica.
Na dilatação térmica linear, a variação mais significativa sofrida pelo corpo envolve apenas uma dimensão, que é o comprimento. Por exemplo, a dilatação térmica em um fio ocorre mais significativamente em seu comprimento do que em outras dimensões. Sendo alpha o coeficiente de dilatação linear, a variação do comprimento é dada por:
Delta L = L_0 alpha Delta theta
Onde L_0 é o comprimento inicial e Delta theta é a variação da temperatura. Da equação acima, temos que:
alpha = dfrac { Delta L } { L_0 Delta theta }
Logo,
alpha = dfrac { Delta L } { L_0 } cdot dfrac { 1 } { Delta theta }
De acordo com o enunciado, temos que { Delta L } / { L_0 } = 0,15% = dfrac {0,15}{100} e Delta theta = 50°C. Assim, temos que:
alpha = dfrac {0,15}{100} cdot dfrac { 1 } { 50 }
alpha = 3 times 10^{-5}
Portanto, a resposta correta é a alternativa (A).
