Questões Sobre Termologia - Física - concurso
911) A tabela a seguir informa o calor específico de algumas substâncias.
- A) se apenas a afirmativa I estiver correta.
- B) se as afirmativas I e III estiverem corretas.
- C) se as afirmativas I e II estiverem corretas.
- D) se as afirmativas II e III estiverem corretas.
- E) se todas as afirmações estiverem corretas.
A alternativa correta é letra B) se as afirmativas I e III estiverem corretas.
Vamos analisar cada uma das alternativas:
I. Atualmente, nos consultórios dentários, são utilizados motores de alta rotação. O atrito entre a broca e o dente provocaria um brutal aumento na temperatura que seria impossível suportar. Para que isso não ocorra, durante o contato entre a broca e o dente, é lançado sobre este um jato contínuo de água. CORRETA.
De fato, o atrito entre a broca provoca um aumento na temperatura, pois a energia mecânica associada ao movimento relativo entre as superfícies em atrito se transforma em energia interna, o que eleva a temperatura do dente. Para resfriá-lo, o dentista precisa utilizar uma substância que possua calor específico elevado, já que o calor retirado é proporcional ao calor específico. Observe que a água é a substância de maior calor específico da tabela. Isso explica o fato da água ser utilizada para resfriamento em vários tipos de perfurações. Alternativa correta.
II. Para resfriar uma peça aquecida, é usual mergulhá-la em água (líquida). Seria muito mais eficiente, para resfriá-la, mergulhá-la em mercúrio. Só não se faz isso porque o mercúrio, além de emitir vapores tóxicos, custa muito caro. INCORRETA.
Como mencionamos no item anterior, para que uma substância seja eficiente no resfriamento, seu calor específico deve ser elevado. Observe na tabela que o mercúrio possui o menor calor específico. Portanto, o mercúrio não é utilizado para resfriamento apenas devido às características citadas, mas também por ter baixo calor específico. Alternativa incorreta.
III. Para esterilizar dois instrumentos cirúrgicos de massas iguais, um de ferro outro de alumínio, inicialmente à temperatura ambiente, colocam-se os dois em um forno durante o mesmo intervalo de tempo, de modo que ambos recebam a mesma quantidade de calor. Nesse caso, a temperatura do instrumento de ferro aumentará o dobro do que aumentar a temperatura do instrumento de alumínio. CORRETA.
O calor sensível, responsável pelo aumento de temperatura, é dado por:
Q=mcDelta theta
Onde m é a massa, c é o calor específico e Delta theta é a variação de temperatura. Como o ferro e o alumínio receberam a mesma quantidade de calor, temos:
m_{Fe} cdot c_{Fe} cdot Delta theta_{Fe} = m_{Al} cdot c_{Al} cdot Delta theta_{Al}
Como as massas são iguais, temos que:
cancel { m_{Fe} } cdot c_{Fe} cdot Delta theta_{Fe} = cancel { m_{Al} } cdot c_{Al} cdot Delta theta_{Al}
c_{Fe} cdot Delta theta_{Fe} = c_{Al} cdot Delta theta_{Al}
Da tabela, temos que c_{Fe} = 0,11 , cal/gºC e c_{Al} = 0,22 , cal/gºC, ou seja, c_{Al} = 2 c_{Fe}. Então, temos:
cancel { c_{Fe} } cdot Delta theta_{Fe} = 2 cancel { c_{Fe} } cdot Delta theta_{Al}
Delta theta_{Fe} = 2 Delta theta_{Al}
Logo, podemos afirmar que a temperatura do instrumento de ferro aumentará o dobro do que aumentar a temperatura do instrumento de alumínio. Alternativa correta.
Portanto, a resposta correta é a alternativa (B).
912) Atenção: Considere as informações abaixo para responder à questão.
- A) 328
- B) 300
- C) 150
- D) 119
A alternativa correta é letra D) 119
A capacidade térmica de um corpo é definida como a quantidade de calor necessária para que sua temperatura aumente em uma unidade. Dessa forma, podemos escrever:
C = dfrac {Q}{Delta theta}
Como Q = mcDelta theta, temos:
C = dfrac {m c cancel {Delta theta}}{cancel {Delta theta}}
C = mc
Assim, a capacidade térmica do sistema é dado por:
C_{sis} = C_{frasco}+C_{água}+C_{latão}
De acordo com o enunciado, o frasco possui capacidade térmica desprezível. Assim, temos:
C_{sis} = C_{água}+C_{latão}
Logo,
C_{sis} = m_{água} cdot c_{água} +m_{latão} cdot c_{água}
C_{sis} = 100 cdot 1 +200 cdot 0,095
C_{sis} = 119 mathrm{ cal/°C}
Portanto, a resposta correta é a alternativa (D).
913) Atenção: Considere as informações abaixo para responder à questão.
- A) 25
- B) 30
- C) 35
- D) 40
A alternativa correta é letra B) 30
Supondo-se que não há troca de calor com o ambiente, devemos ter:
Q_{água} + Q_{latão} = 0
Como Q = mcDelta theta, temos:
m_{água} cdot c_{água} cdot (theta_e - theta_{água} ) + m_{latão} cdot c_{latão} cdot (theta_e - theta_{latão} ) = 0
Onde theta_e é a temperatura de equilíbrio. Dessa forma, temos:
100 cdot 1 cdot (theta_e - 20 ) + 200 cdot 0,095 cdot (theta_e - 80) = 0
100 theta_e - 2000 + 19theta_e - 1520 = 0
119 theta_e = 3520
theta_e approx 29,58 °C
Portanto, a resposta correta é a alternativa (B).
914) Considere que uma placa metálica que, inicialmente, está a 100 ºC seja submetida a resfriamento por ar a temperatura de 40 ºC até atingir o equilíbrio térmico.
- A) Certo
- B) Errado
A alternativa correta é letra A) Certo
ITEM CORRETO
Considerando uma área de 1m^2, temos:
Fluxo = frac{Delta Q}{Delta t}= h.A.Delta T=100.1.60=6000W.m^{-2}
915) Um isolante térmico de 10 cm de espessura e condutividade térmica igual a 20 W • m–1 • K–1 apresenta a temperatura da superfície quente igual a 80 ºC e a da superfície fria igual a 30 ºC.
- A) Certo
- B) Errado
A alternativa correta é letra B) Errado
A questão afirma que o fluxo de calor por unidade de área é igual a 16 kW • m–2
Dados da questão
Um isolante térmico de 10 cm ( 0,1m )de espessura
condutividade térmica igual a 20 W • m–1 • K–1
temperatura da superfície quente igual a 80 ºC (353K)
temperatura da superfície da superfície fria igual a 30 ºC (303K)
Substituindo os valores na equação do fluxo de calor, temos:
frac{Phi}{A}=frac{K.Delta T}{L}
frac{Phi}{A}=frac{20.(353-303)}{0,1}= 10000=10kW.m^{-2}.
GABARITO ERRADO
916) Com relação aos princípios da termodinâmica, julgue o item subsequente.
- A) Certo
- B) Errado
A alternativa correta é letra A) Certo
De acordo com a lei de Stefan-Boltzmann, a radiação do corpo negro é dada por:
R = sigma T^4
Onde sigma é a constante de Stefan-Boltzmann e T é a temperatura do corpo.
O gráfico di-log consiste na representação gráfica de dados que estão relacionados exponencialmente, de forma que ambos os eixos estão em escala logarítmica. Para isso, podemos realizar uma mudança de variável, aplicando o logarítmo em ambos os lados da equação:
R = sigma T^4
log R = log ( sigma T^4 )
log R = log sigma + log T^4
log R = log sigma + 4 log T
Fazendo log R = R', log T = T' e log sigma = c, temos a seguinte equação:
R' = c + 4 T'
Assim, podemos afirmar que o gráfico di-log da potência da radiação eletromagnética dissipada por um corpo negro versus a temperatura do corpo é uma reta de coeficiente angular 4.
Resposta: CERTO.
Questão 917
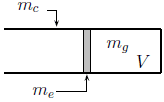
- A) ( ) 3PV^γ/2.
- B) ( ) 3PV/(2(γ-1)).
- C) ( ) -m_c(m_e + m_c)v^2_c/(2m_e).
- D) ( ) -(m_c + m_e)v^2_c/2.
- E) ( ) -m_e(m_e + m_c)v^2_c/(2m_c).
A alternativa correta é letra C) ( ) -m_c(m_e + m_c)v^2_c/(2m_e).
De acordo com a primeira lei da termodinâmica, temos:
Delta U = Q - W
Como o gás expande-se adiabaticamente, temos que Q = 0. Logo,
Delta U = - W
Assim, podemos afirmar que ao liberar o êmbolo, a variação da energia interna do gás será convertida em trabalho para deslocar o êmbolo. Como não há atrito, esse trabalho é totalmente utilizado fornecer energia cinética aos componentes do sistema. Então, temos:
Delta U = - W = - E_{cin}^{sis}
Como as massas do cilindro e do êmbolo são muito maiores que a massa do gás, temos:
Delta U = - ( E_{cin}^{embolo} +E_{cin}^{cilindro} )
Delta U = - left( dfrac {m_e cdot {v_e}^2}{2} + dfrac {m_c cdot {v_c}^2}{2} right)
De acordo com a lei da conservação do momento, temos:
Q_{antes} = Q_{depois}
Como o sistema parte do repouso, temos que Q_{antes} = 0. Logo,
Q_{depois} = 0
Assim, temos:
m_c cdot v_c + m_e cdot v_e = 0
Então,
m_e cdot v_e = - m_c cdot v_c
v_e = - dfrac {m_c cdot v_c}{m_e }
Então, a variação da energia interna ΔU do gás quando a velocidade do cilindro for v_c é dada aproximadamente por:
Delta U = - left( dfrac {m_e cdot left( - dfrac {m_c cdot v_c}{m_e } right)^2}{2} + dfrac {m_c cdot {v_c}^2}{2} right)
Delta U = - left( dfrac { cancel {m_e} cdot dfrac { {m_c}^2 cdot {v_c}^2 } { {m_e}^{cancel 2} } }{2} + dfrac {m_c cdot {v_c}^2}{2} right)
Delta U = - left( dfrac { {m_c}^2 cdot {v_c}^2 } { 2 m_e } + dfrac {m_c cdot {v_c}^2}{2} right)
Delta U = - left( dfrac { {m_c}^2 cdot {v_c}^2 + m_c cdot m_e cdot {v_c}^2}{ 2 m_e } right)
Delta U = - dfrac { m_c ( m_c cdot {v_c}^2 + m_e cdot {v_c}^2)}{ 2 m_e }
Delta U = - dfrac { m_c cdot (m_c + m_e) cdot {v_c}^2}{ 2 m_e }
Portanto, a resposta correta é a alternativa (C).
918) Assinale a opção que apresenta a afirmação CORRETA.
- A) ( ) Um paciente com calor de 42ºC apresenta-se febril.
- B) ( ) A adição de energia térmica à água líquida em ebulição sob pressão ambiente causa um aumento na sua capacidade calorífica.
- C) ( ) Na temperatura de - 4ºC e pressão ambiente, 5 g de água no estado líquido contêm uma quantidade de energia maior do que a de 5 g de água no estado sólido.
- D) ( ) A quantidade de energia necessária para aquecer 5 g de água de 20ºC até 25ºC é igual àquela necessária para aquecer 25 g de água no mesmo intervalo de temperatura e pressão ambiente.
- E) ( ) Sob pressão ambiente, a quantidade de energia necessária para aquecer massas iguais de alumínio (calor específico 0,89,J·g^{-1}·K^{-1}) e de ferro (calor específico 0,45,J·g^{-1}·K^{-1}), respectivamente, de um mesmo incremento de temperatura,ΔT, é aproximadamente igual.
A alternativa correta é letra C) ( ) Na temperatura de - 4ºC e pressão ambiente, 5 g de água no estado líquido contêm uma quantidade de energia maior do que a de 5 g de água no estado sólido.
ALTERNATIVA CORRETA: LETRA C
a) ( ) Um paciente com calor de 42ºC apresenta-se febril.
ERRADA:
O paciente deve ter uma temperatura de 42°C e não calor de 42°C.
b) ( ) A adição de energia térmica à água líquida em ebulição sob pressão ambiente causa um aumento na sua capacidade calorífica.
ERRADA:
No processo de ebulição de uma substância pura, como a água, não há mudança nos valores das propriedades termodinâmicas.
A capacidade calorífica da água depende da temperatura, mas na ebulição a temperatura permanece constante.
c) ( ) Na temperatura de - 4ºC e pressão ambiente, 5 g de água no estado líquido contêm uma quantidade de energia maior do que a de 5 g de água no estado sólido.
CORRETA:
A mesma massa de uma substância, nas mesma condições de pressão e temperatura, conterá maior energia no seu estado líquido, no caso o material deve absorver energia para passar do estado sólido para o líquido.
d) ( ) A quantidade de energia necessária para aquecer 5 g de água de 20ºC até 25ºC é igual àquela necessária para aquecer 25 g de água no mesmo intervalo de temperatura e pressão ambiente.
ERRADA:
A quantidade de energia depende do material, da massa e da variação de temperatura. Como a massa de uma amostra é cinco vezes maior, a quantidade de energia para 25g é cinco vezes maior.
Q_{m=25g}=5.Q_{m=5g}
e) ( ) Sob pressão ambiente, a quantidade de energia necessária para aquecer massas iguais de alumínio (calor específico 0,89,J·g^{-1}·K^{-1}) e de ferro (calor específico 0,45,J·g^{-1}·K^{-1}), respectivamente, de um mesmo incremento de temperatura, ΔT, é aproximadamente igual.
ERRADA:
A quantidade de energia necessária é dada pela expressão: Q=m.C_p.Delta T
Para massas iguais terem a mesma variação de temperatura, a espécie que tem o maior calor específico deverá receber mais energia, ou seja, a energia fornecida ao alumínio deverá ser maior.
ALTERNATIVA CORRETA: LETRA C
919) Com relação aos mecanismos de troca de calor que ocorrem no interior de uma garrafa térmica, é correto afirmar que:
- A) o vácuo feito nas paredes da garrafa térmica contribui para que a radiação térmica não se propague, evitando a retirada ou entrada de calor no dispositivo térmico.
- B) a superfície de plástico da garrafa térmica é um ótimo isolante térmico que evita que o calor seja transportado por condução no dispositivo térmico.
- C) as superfícies espelhadas no interior da garrafa térmica favorecem o confinamento da radiação térmica contida no interior do dispositivo térmico.
- D) as conexões de borracha da garrafa térmica funcionam como isolantes que blindam a radiação térmica, evitando que o calor saia ou entre no dispositivo térmico.
- E) as correntes de convecção que existem entre as paredes externas da garrafa térmica conduzem calor na região de vácuo existente no dispositivo térmico.
Resposta: A alternativa correta é a letra C) as superfícies espelhadas no interior da garrafa térmica favorecem o confinamento da radiação térmica contida no interior do dispositivo térmico.
A garrafa térmica é um dispositivo projetado para manter a temperatura de um líquido ou de um corpo por um período de tempo prolongado. Para alcançar esse objetivo, garrafa térmica utiliza vários mecanismos de troca de calor, incluindo a radiação térmica. A radiação térmica é uma forma de transferência de calor que ocorre por meio da emissão e absorção de ondas eletromagnéticas.
No interior da garrafa térmica, as superfícies espelhadas desempenham um papel fundamental no confinamento da radiação térmica. Essas superfícies espelhadas são projetadas para refletir a radiação térmica de volta para o interior do dispositivo térmico, evitando que ela escape. Isso ajuda a manter a temperatura do líquido ou do corpo dentro da garrafa térmica.
Além disso, as superfícies espelhadas também ajudam a reduzir a perda de calor por condução e convecção. Isso ocorre porque as superfícies espelhadas reduzem a área de contato entre o interior e o exterior da garrafa térmica, minimizando a perda de calor por condução. Além disso, as superfícies espelhadas também ajudam a reduzir a convecção natural, pois elas criam uma barreira que impede o fluxo de ar entre o interior e o exterior da garrafa térmica.
Portanto, as superfícies espelhadas no interior da garrafa térmica são fundamentais para o confinamento da radiação térmica e para a manutenção da temperatura do líquido ou do corpo dentro do dispositivo térmico.
920) Uma das maiores temperaturas já registradas no Brasil foi de +44,7º C, no dia 21 de novembro de 2005, na cidade de Bom Jesus, no Piauí. Já uma das temperaturas mais baixas registradas no Brasil foi de –14º C, no dia 11 de junho de 1952, na cidade de Caçador, em Santa Catarina. Quais são, respectivamente, os valores da maior e da menor temperatura já registradas no Brasil conforme o sistema internacional de unidades (SI)?
- A) 317.85 Kelvin, 259.15 Kelvin.
- B) 259.15 Kelvin, 120.85 Kelvin.
- C) 359.15º Fahrenheit e 217.85º Fahrenheit.
- D) 359.15º Fahrenheit e 82º Fahrenheit.
- E) 359.15 Kelvin, –207.85 Kelvin.
A resposta correta é a letra A) 317.85 Kelvin, 259.15 Kelvin.
Para entendermos a razão pela qual essa é a resposta correta, precisamos lembrar que a temperatura em graus Celsius pode ser convertida para Kelvin utilizando a fórmula: K = °C + 273.15. Sendo assim, para calcular a temperatura em Kelvin correspondente à temperatura de +44,7°C, basta substituir o valor de °C na fórmula:
Já para calcular a temperatura em Kelvin correspondente à temperatura de -14°C, fazemos o mesmo:
Portanto, as temperaturas de +44,7°C e -14°C correspondem, respectivamente, às temperaturas de 317.85 K e 259.15 K no sistema internacional de unidades (SI).
