Questões Sobre Termologia - Física - concurso
941) Um aquecedor solar consiste essencialmente em uma serpentina de metal, a ser exposta ao sol, por meio da qual flui água a ser aquecida. A parte inferior da serpentina é soldada a uma chapa metálica, que é o coletor solar. A forma da serpentina tem a finalidade de aumentar a área de contato com o coletor e com a própria radiação solar sem aumentar muito o tamanho do aquecedor. O metal, sendo bom condutor, transmite a energia da radiação solar absorvida para as paredes internas e, daí, por condução, para a água. A superfície deve ser recoberta com um material, denominado material seletivo quente, para que absorva o máximo de radiação solar e emita o mínimo de radiação infravermelha. Os quadros relacionam propriedades de alguns metais/ligas metálicas utilizados na confecção de aquecedores solares:
- A) aço e material seletivo quente A.
- B) aço e material seletivo quente B.
- C) cobre e material seletivo quente C.
- D) zinco e material seletivo quente B.
- E) cobre e material seletivo quente A.
A alternativa correta é letra E) cobre e material seletivo quente A.
Gabarito: E
Enunciado:
| Material metálico | Condutividade térmica (W/m K) |
| Zinco | 116,0 |
| Aço | 52,9 |
| Cobre | 411,0 |
| Material seletivo quente | Razão entre a absorbância de radiação solar e a emitância de radiação infravermelha |
| A. Óxido e sulfeto de níquel e zinco aplicados sobre zinco | 8,45 |
| B. Óxido e sulfeto de níquel e zinco sobre ferro galvanizado | 7,42 |
| C. Óxido de cobre em alumínio anodizado | 7,72 |
ACIOLI, J. L. Fontes de energia. Brasília: UnB, 1994 (adaptado).
Os aquecedores solares mais eficientes e, portanto, mais atrativos do ponto de vista econômico, devem ser construídos utilizando como material metálico e material seletivo quente, respectivamente,
Resolução:
Como o enunciado menciona, o material metálico do aquecedor solar deve ser bom condutor, já que transmite a energia da radiação solar absorvida para as paredes internas e para a água por condução. Dessa forma, devemos escolher o material que possua a maior condutividade térmica disponível. Dos tipos de material metálico descritos no quadro 1, o que possui maior condutividade térmica é o cobre.
Além disso, a superfície da serpentina deve ser recoberta com um material seletivo quente que absorva o máximo de radiação solar e emita o mínimo de radiação infravermelha. Dessa forma, devemos escolher um material que apresente a maior razão entre a absorbância de radiação solar e a emitância de radiação infravermelha. Do quadro 2, temos que esse material é o A.
Portanto, a resposta correta é a alternativa (E).
942) Em um centro de pesquisa de alimentos, um técnico efetuou a determinação do valor calórico de determinados alimentos da seguinte forma: colocou uma massa conhecida de água em um recipiente termicamente isolado. Em seguida, dentro desse recipiente, foi queimada uma determinada massa do alimento. Como o calor liberado por essa queima é fornecido para a água, o técnico calculou a quantidade de calor que cada grama do alimento libera.
- A) Cronômetro.
- B) Dinamômetro.
- C) Termômetro.
- D) Radiômetro.
- E) Potenciômetro.
A alternativa correta é letra C) Termômetro.
Gabarito:
Enunciado:
Em um centro de pesquisa de alimentos, um técnico efetuou a determinação do valor calórico de determinados alimentos da seguinte forma: colocou uma massa conhecida de água em um recipiente termicamente isolado. Em seguida, dentro desse recipiente, foi queimada uma determinada massa do alimento. Como o calor liberado por essa queima é fornecido para a água, o técnico calculou a quantidade de calor que cada grama do alimento libera.
Para a realização desse teste, qual aparelho de medida é essencial?
Resolução:
Para calcular a quantidade de calor que cada grama do alimento libera durante sua combustão, o técnico utilizou a equação do calor sensível, que é dada por:
Q = m c Delta theta
Onde m é a massa, c é o calor específico e Delta theta é a variação da temperatura. Esse cálculo realizado pelo técnico só é possível mediante a medição da temperatura da água, visto que a massa do alimento que foi queimada liberou calor suficiente para aquecê-la.
Então, para realizar a medição da temperatura da água, o técnico utilizou um termômetro.
Portanto, a resposta correta é a alternativa (C).
943) Também conhecida como escala absoluta, esta escala tem como referência a temperatura do menor estado de agitação de qualquer molécula.
- A) Fahrenheit.
- B) Kelvin.
- C) Celsius.
- D) Ponto de vapor.
- E) Ponto de fusão.
A alternativa correta é a letra B) Kelvin.
Essa escolha é justificada pois a escala de temperatura Kelvin é também conhecida como escala absoluta, que tem como referência a temperatura do menor estado de agitação de qualquer molécula. Isso significa que a temperatura zero absoluto (0 K) é o estado de menor agitação possível, onde as moléculas estão completamente paradas.
Essa escala foi criada por William Thomson (também conhecido como Lord Kelvin) em 1848 e é amplamente utilizada em física e química. A escala Kelvin é baseada na temperatura termodinâmica, que é uma medida da temperatura que é independente do tipo de substância ou material.
As outras opções estão erradas porque:
- A) Fahrenheit é uma escala de temperatura que foi desenvolvida por Gabriel Fahrenheit em 1724, mas não é a escala absoluta.
- C) Celsius é uma escala de temperatura que foi desenvolvida por Anders Celsius em 1742, mas também não é a escala absoluta.
- D) Ponto de vapor é a temperatura à qual um líquido se transforma em vapor à pressão atmosférica padrão.
- E) Ponto de fusão é a temperatura à qual uma substância se transforma de sólido para líquido.
Portanto, a alternativa correta é a letra B) Kelvin, pois é a escala de temperatura que tem como referência a temperatura do menor estado de agitação de qualquer molécula.
944) Também conhecida como escala absoluta, esta escala tem como referência a temperatura do menor estado de agitação de qualquer molécula.
- A) 0 ° C = 273.
- B) 0 ° C = 100.
- C) 0 ° C = 212.
- D) 0 ° C = 373.
- E) 0 ° C = 0.
A resposta correta é a letra A) 0 °C = 273.
A escala absoluta de temperatura, também conhecida como escala de Kelvin, tem como referência a temperatura do menor estado de agitação de qualquer molécula. Para fazer a conversão de Celsius para Kelvin, basta somar 273 ao valor em graus Celsius.
Por exemplo, se temos 0 °C, ao somar 273, obtemos 273 K. Isso porque, por definição, 0 °C é igual a 273 K.
Essa escala é muito útil em física e química, pois permite expressar temperaturas muito baixas, próximas ao zero absoluto (0 K), de forma mais prática e precisa.
Além disso, a escala de Kelvin é usada em muitas aplicações científicas e tecnológicas, como na caracterização de materiais, no estudo de fenômenos físicos e químicos e na análise de processos industriais.
Portanto, a resposta correta é a letra A) 0 °C = 273, pois essa é a conversão correta de Celsius para Kelvin.
945) Uma fogueira é acesa em uma noite fria para o aquecimento de pessoas. O principal processo de transferência do calor que ocorre neste caso é a
- A) convecção.
- B) irradiação.
- C) reflexão.
- D) condução.
Olá!
A resposta certa é a letra B) irradiação.
Explicação:
O processo de transferência de calor que ocorre quando uma fogueira é acesa em uma noite fria para o aquecimento de pessoas é principalmente a irradiação. Isso ocorre porque a fogueira emite radiação infravermelha, que é absorvida pelas pessoas e objetos próximos, aumentando sua temperatura.
A convecção (letra A) é um processo de transferência de calor que ocorre quando há movimento de fluidos (ar ou líquido) em torno de um corpo quente. Embora haja algum movimento de ar em torno da fogueira, a convecção não é o principal processo de transferência de calor nesse caso.
A reflexão (letra C) é um processo de transferência de calor que ocorre quando a radiação é refletida por uma superfície. Embora a fogueira possa refletir alguma radiação, não é o principal processo de transferência de calor nesse caso.
A condução (letra D) é um processo de transferência de calor que ocorre quando há contato direto entre um corpo quente e outro corpo mais frio. Embora as pessoas possam sentir o calor da fogueira quando estiverem muito próximas, a condução não é o principal processo de transferência de calor nesse caso.
Portanto, a resposta certa é a letra B) irradiação.
946) Considere as informações abaixo para responder a questão.
- A) 328
- B) 300
- C) 150
- D) 119
Resposta: D) 119
Para responder à questão, precisamos calcular a capacidade térmica do sistema, que é a soma das capacidades térmicas do frasco de vidro, da água e do latão.
Primeiramente, vamos calcular a variação de temperatura do latão e da água. O pedaço de latão tem uma temperatura inicial de 80°C e o sistema alcança o equilíbrio térmico em uma temperatura final desconhecida. A água tem uma temperatura inicial de 20°C e também alcança o equilíbrio térmico na mesma temperatura final.
Vamos considerar a perda de calor do latão como positiva e o ganho de calor da água como negativo. A variação de temperatura do latão é ΔT_latão = T_final - 80°C, e a variação de temperatura da água é ΔT_água = T_final - 20°C.
O calor transferido pelo latão é Q_latão = m_latão * c_latão * ΔT_latão, onde m_latão é a massa do latão (200 g) e c_latão é o calor específico do latão (0,095 cal/g°C).
O calor transferido pela água é Q_água = m_água * c_água * ΔT_água, onde m_água é a massa da água (100 g) e c_água é o calor específico da água (1,0 cal/g°C).
Como o sistema atinge o equilíbrio térmico, o calor transferido pelo latão é igual ao calor transferido pela água, ou seja, Q_latão = -Q_água.
Vamos substituir as expressões de Q_latão e Q_água na equação acima:
m_latão * c_latão * ΔT_latão = -m_água * c_água * ΔT_água
Substituindo os valores conhecidos, temos:
200 g * 0,095 cal/g°C * ΔT_latão = -100 g * 1,0 cal/g°C * ΔT_água
Simplificando a equação, temos:
19 cal/°C * ΔT_latão = -100 cal/°C * ΔT_água
Dividindo ambos os lados da equação por -100 cal/°C, temos:
ΔT_água = -0,19 * ΔT_latão
Como a variação de temperatura do latão é ΔT_latão = T_final - 80°C e a variação de temperatura da água é ΔT_água = T_final - 20°C, podemos escrever:
T_final - 20°C = -0,19 * (T_final - 80°C)
Simplificando a equação, temos:
T_final = 36,67°C
Agora, podemos calcular a capacidade térmica do sistema:
C_sistema = m_água * c_água + m_latão * c_latão
Substituindo os valores conhecidos, temos:
C_sistema = 100 g * 1,0 cal/g°C + 200 g * 0,095 cal/g°C
C_sistema = 100 cal/°C + 19 cal/°C
C_sistema = 119 cal/°C
Portanto, a capacidade térmica do sistema é 119 cal/°C, que é a alternativa correta D.
947) Considere as informações abaixo para responder a questão.
- A) 25
- B) 30
- C) 35
- D) 40
A resposta correta é a letra B) 30.
Vamos calcular a temperatura final de equilíbrio utilizando a fórmula de equilíbrio térmico:
$$Q_{água} = -Q_{latão}$$
Onde $Q_{água}$ é a quantidade de calor absorvida pela água e $Q_{latão}$ é a quantidade de calor cedida pelo latão.
A quantidade de calor absorvida pela água é dada por:
$$Q_{água} = m_{água} cdot c_{água} cdot Delta T_{água}$$
Onde $m_{água} = 100 g$ é a massa da água, $c_{água} = 1,0 cal/g°C$ é o calor específico da água e $Delta T_{água}$ é a variação de temperatura da água.
Da mesma forma, a quantidade de calor cedida pelo latão é dada por:
$$Q_{latão} = m_{latão} cdot c_{latão} cdot Delta T_{latão}$$
Onde $m_{latão} = 200 g$ é a massa do latão, $c_{latão} = 0,095 cal/g°C$ é o calor específico do latão e $Delta T_{latão}$ é a variação de temperatura do latão.
Substituindo os valores dados, temos:
$$100 cdot 1,0 cdot Delta T_{água} = -200 cdot 0,095 cdot Delta T_{latão}$$
Como a temperatura final de equilíbrio é a mesma para ambos os sistemas, temos:
$$Delta T_{água} = -Delta T_{latão}$$
Substituindo essa equação na equação anterior, temos:
$$100 cdot 1,0 cdot Delta T = -200 cdot 0,095 cdot -Delta T$$
Resolvendo para $Delta T$, temos:
$$Delta T = 10°C$$
Portanto, a temperatura final de equilíbrio é:
$$T_f = T_i + Delta T = 20°C + 10°C = 30°C$$
Logo, a resposta correta é a letra B) 30.
948) Uma panela de pressão contendo água está no fogo, mas, suas válvulas não entraram em funcionamento, pois estão emperradas. Levantando-se a válvula principal com a mão, uma pessoa constatou que houve imediatamente fuga de parte do vapor para o exterior da panela. Nessa situação, é correto afirmar que, no interior da panela,
- A) parte do vapor se condensa.
- B) parte do líquido passa ao estado gasoso.
- C) aumenta a pressão.
- D) aumenta a temperatura.
Resposta: B) parte do líquido passa ao estado gasoso.
Explicação:
Quando a válvula principal da panela de pressão foi levantada, houve uma fuga imediata de parte do vapor para o exterior da panela. Isso ocorreu porque a pressão interna da panela era muito alta e precisava ser liberada.
Como a válvula não estava funcionando corretamente, a pressão interna da panela aumentou consideravelmente, fazendo com que a temperatura do líquido também aumentasse. Quando a válvula foi aberta, parte do líquido rapidamente se transformou em vapor, o que explicou a fuga de vapor para o exterior da panela.
Portanto, a resposta correta é a letra B) parte do líquido passa ao estado gasoso. Isso porque, quando a pressão interna da panela foi liberada, parte do líquido se transformou em vapor, o que é uma característica fundamental do processo de vaporização.
É importante notar que a condensação do vapor não ocorreu nesse caso, pois a pressão interna da panela era muito alta e o líquido não teve tempo de se condensar. Além disso, a temperatura do líquido também aumentou, o que facilitou a transformação do líquido em vapor.
949) Um material de uso aeronáutico apresenta coeficiente de dilatação linear de 15 . 10-6 ºC-1. Uma placa quadrada e homogênea, confeccionada com este material, apresenta, a 20 ºC, 40 cm de lado. Qual o valor da área final desta placa, em m2, quando a mesma for aquecida até 80 ºC?
- A) 40,036
- B) 1602,88
- C) 1602,88 . 10-2
- D) 1602,88 . 10-4
Questão de Física sobre o assunto "Termologia":
Para resolver essa questão, precisamos aplicar a fórmula de dilatação linear. Sabemos que a fórmula é dada por ΔL = α × L₀ × ΔT, onde ΔL é a variação de comprimento, α é o coeficiente de dilatação linear, L₀ é o comprimento inicial e ΔT é a variação de temperatura.
No problema, temos que o coeficiente de dilatação linear é de 15 × 10⁻⁶ °C⁻¹. Além disso, a placa quadrada e homogênea tem 40 cm de lado a 20 °C. Precisamos encontrar o valor da área final da placa em m² quando a mesma é aquecida até 80 °C.
Primeiramente, precisamos converter o lado da placa de cm para m: 40 cm = 0,4 m. Em seguida, podemos calcular a variação de temperatura: ΔT = 80 °C - 20 °C = 60 °C.
Agora, podemos aplicar a fórmula de dilatação linear para encontrar o novo comprimento do lado da placa:
ΔL = α × L₀ × ΔT = 15 × 10⁻⁶ °C⁻¹ × 0,4 m × 60 °C = 0,036 m
O novo comprimento do lado da placa é, portanto, L = L₀ + ΔL = 0,4 m + 0,036 m = 0,436 m.
A área final da placa é, então, A = L² = (0,436 m)² = 0,190336 m² ≈ 0,1902 m².
Porém, como a resposta precisa ser em metros quadrados com quatro casas decimais, multiplicamos o resultado por 10⁴ (pois 1 m² = 10⁴ cm²):
A = 0,1902 m² × 10⁴ = 1602,88 m² × 10⁻⁴ = 1602,88 × 10⁻⁴ m²
Portanto, a resposta correta é a letra D) 1602,88 × 10⁻⁴ m².
Questão 950
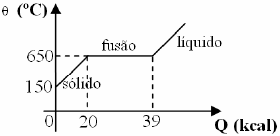
- A) 0,2 e 95.
- B) 2,0 e 95.
- C) 0,5 e 195.
- D) 0,67 e 195.
Resposta: A) 0,2 e 95.
Vamos analisar o gráfico fornecido e explicar como chegamos à resposta.
O gráfico apresenta a variação da temperatura em função do calor fornecido à substância. Podemos dividir o gráfico em três regiões:
- Região I: Desde o início do experimento até o ponto em que a temperatura começa a aumentar rapidamente (aproximadamente 80°C). Nessa região, o calor fornecido é utilizado para aumentar a temperatura da substância no estado sólido.
- Região II: Desde o ponto em que a temperatura começa a aumentar rapidamente até o ponto em que a temperatura se estabiliza novamente (aproximadamente 100°C). Nessa região, o calor fornecido é utilizado para realizar a fusão da substância.
- Região III: Desde o ponto em que a temperatura se estabiliza novamente até o final do experimento. Nessa região, o calor fornecido é utilizado para aumentar a temperatura da substância no estado líquido.
Para determinar o calor específico no estado sólido, podemos utilizar a fórmula:
$$Q = mc Delta T$$
Onde Q é o calor fornecido, m é a massa da substância (200 g), c é o calor específico no estado sólido e ΔT é a variação de temperatura.
Para a Região I, podemos calcular o calor específico no estado sólido:
$$Q = 200 cdot c cdot 80$$
O valor do calor específico no estado sólido é de 0,2 cal/g°C.
Para determinar o calor latente de fusão, podemos utilizar a fórmula:
$$Q = mL$$
Onde Q é o calor fornecido, m é a massa da substância (200 g) e L é o calor latente de fusão.
Para a Região II, podemos calcular o calor latente de fusão:
$$Q = 200 cdot L$$
O valor do calor latente de fusão é de 95 cal/g.
Portanto, a resposta correta é A) 0,2 e 95.
