Sabendo-se que o calor de fusão do gelo é igual a 80 cal/g, que o calor de vaporização da água é igual a 540 cal/g, que o calor específico do vapor da água é igual a 0,50 cal/g e que o calor específico da água líquida é igual a 1 cal/g ºC, é correto afirmar que a quantidade de calor necessária para transformar 30 g de gelo a 0 ºC em vapor d’água a 150 ºC é
- A) 2,40 times 10^3 mbox{ cal}.
- B) 7,50 times 10^2 mbox{ cal}.
- C) 22,35 times 10^3 mbox{ cal}.
- D) 21,60 times 10^3 mbox{ cal}.
- E) 5,40 times 10^3 mbox{ cal}.
Resposta:
A alternativa correta é letra C)
22,35 times 10^3 mbox{ cal}.
Abaixo temos a curva de aquecimento. Ela demonstra a variação da temperatura de um corpo,quando este recebe calor.
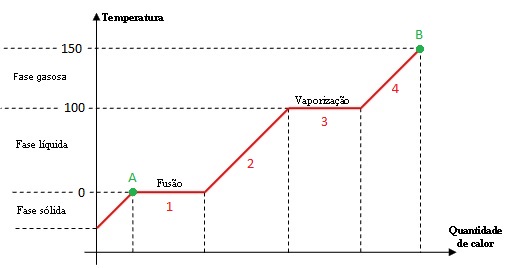
O corpo se encontra inicialmente no estado sólido (ponto A) e receberá calor até chegar ao estado representado pelo ponto (B).
1 - Fusão
Q_1 = m cdot L
Q_1 = 30 cdot 80 = 2400 cal
2 - Aquecimento do líquido
Q_2 = m cdot c cdot Delta T
Q_2 = 30 cdot 1 cdot 100 = 3000 mbox{ cal}
3 - Vaporização
Q_3 = m cdot L
Q_3 = 30 cdot 540 = 16200 mbox{ cal}
4 - Aquecimento do vapor
Q_4 = m cdot c cdot Delta T
Q_4 = 30 cdot 0,5 cdot 50 = 750 mbox{ cal}
Total
Q = Q_1 + Q_2 + Q_3 + Q_4
Q =2400 + 3000 + 16200+ 750 = 22350 mbox{ cal}
Resposta: Alternativa C

Deixe um comentário