Um gás ideal sofreu uma transformação, progredindo estado A, para o estado B posteriormente para o estado C e finalmente para o estado D, conforme indicado no gráfico abaixo:
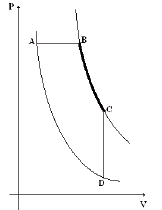
Assinale, entre as opções, aquele que representa corretamente essa mesma transformação.
- A)
- B)
- C)
- D)
- E)
Resposta:
A alternativa correta é letra C)
Resposta: Alternativa C
Transformação A → B: trata-se de uma transformação onde a pressão permaneceu constante (isobárica).
Tal transformação foi estudada pelo físico francês Jacques Charles, o qual constatou que nas transformações gasosas com pressão constante, o volume e a temperatura absoluta (em kelvin) são diretamente proporcionais (Lei de Charles). Logo, o gráfico será uma reta crescente.
Matematicamente:
P cdot V = n cdot R cdot T (equação de Clapeyron)
{V over T} = {n cdot R over P} = mbox{ constante}, pois n, R e P são constantes
Quando a razão entre 2 grandezas é constante, temos uma relação diretamente proporcional e o gráfico será um reta crescente.
Transformação B → C: A curva BC representada no gráfico do enunciado é chamada de isoterma e representa uma transformação onde a temperatura permanece constante. Logo, o gráfico será:
Transformação C → D: Trata-se de uma transformação em que o volume permaneceu constante (isocórica, isométrica ou isovolumétrica). Logo, o gráfico será:
Sobrepondo o gráfico das três transformações, temos:


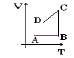



Deixe um comentário