Uma certa quantidade de gás ideal absorve uma certa quantidade de calor, de forma que, durante a expansão, o êmbolo se move sem nenhum tipo de atrito.
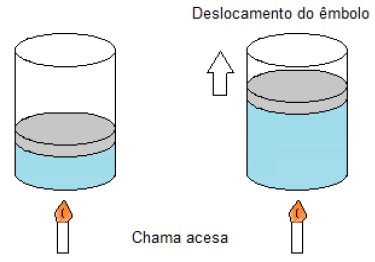
Disponível em: https://www.infoescola.com/termodinamica/transformacoesgasosas. Acesso em: 15 out. 2019.
Admitindo que todo o calor absorvido pelo gás foi utilizado para a realização de trabalho, é CORRETO afirmar que a transformação gasosa descrita na situação é uma:
- A) Transformação isotérmica.
- B) Transformação isobárica.
- C) Transformação adiabática.
- D) Transformação isocórica.
Resposta:
A alternativa correta é letra A) Transformação isotérmica.
A quantidade de calor (Q) fornecida a um sistema é igual ao trabalho realizado pelo gás (tau) mais a variação da energia interna (Delta U) sofrida por ele.
Q=tau + Delta U
A energia interna de um gás depende exclusivamente de sua temperatura. Como todo o calor absorvido pelo gás foi utilizado para a realização de trabalho, podemos afirmar que não houve variação da temperatura interna do gás. Neste caso, teremos uma transformação isotérmica.
Analisemos as alternativas:
Admitindo que todo o calor absorvido pelo gás foi utilizado para a realização de trabalho, é CORRETO afirmar que a transformação gasosa descrita na situação é uma:
a) Transformação isotérmica. Correta a assertiva.
b) Transformação isobárica. Falsa. Transformação isobárica é quando a pressão do sistema permanece constante.
c) Transformação adiabática. Falsa. Transformações adiabáticas são processos termodinâmicos nos quais não ocorrem transferências de calor entre um sistema e suas vizinhanças.
d) Transformação isocórica. Falsa. A transformação isocórica é aquela em que, num processo termodinâmico de um gás ideal, o volume permanece constante durante o processo.
Gabarito: A

Deixe um comentário