Simulado de Ciências da Natureza - 3º ano do ensino médio
Questão 161

Disponível em: http://brasilescola.uol.com.br/quimica/qui mica/química-cafeina.htm. Acesso em: 30 mar.2016.
Considerando a molécula da cafeína, as funções orgânicas presentes são
- A) éter e amina.
- B) fenol e amida.
- C) amina e amida.
- D) cetona e amina.
- E) álcool e amina.
A resposta correta é a letra C)

Questão 162

Disponível em: http://qnesc.sbq.org.br/ online/qnesc34_1/05-EA-43-11.pdf. Acesso em: 24 abr. 2017.
Em sua estrutura química, existem as funções orgânicas éster, enol e
- A) éter.
- B) álcool.
- C) cetona.
- D) aldeído.
- E) hidrocarboneto.
A resposta correta é a letra B)

Questão 163

Relacione as figuras I, II, III e IV com a sequência correta de funções inorgânicas que elas representam:
- A) Ácido, Sal, Base e Óxido
- B) Ácido, Base, Sal e Óxido
- C) Sal, Base, Óxido e Ácido
- D) Ácido, Óxido, Sal e Base
- E) Óxido, Sal, Base e Ácido
A resposta correta é a letra B)
164) Calcular valores de pH e pOH, a partir de concentrações de H₃O⁺ e OH⁻.
- A) pH = 0,30
- B) pH = 3,00
- C) pH = 2,70
- D) pH = 27
- E) pH = −3,00
A resposta correta é a letra C)
DADOS: log 2 = 0,30 e H⁺ = 0,002 mol/L
pH = −log [H⁺]
pH = − log [0,002]
pH = −log [2 × 10⁻³]
pH = − {log 2 + log 10⁻³}
pH = − {log 2 + (−3) ∙ log 10}
pH = − {0,30 + (−3) ∙ 1}
pH = − {0,30 −3}
pH = − {−2,7}
pH = 2,7
Questão 165

Sobre a concentração do refresco preparado, de acordo com as quantidades fornecidas pela embalagem, é correto afirmar que:
- A) Meio litro desse suco, após ter sido preparado nas condições especificadas acima, terá uma concentração de 5 g/L.
- B) Um copo de 100 mL desse suco, após ter sido preparado nas condições especificadas acima, terá uma concentração de 1 g/L.
- C) Um copo de 100 mL desse suco, após ter sido preparado nas condições especificadas acima, terá uma concentração de 10 g/L.
- D) Se tivesse completado para 2 litros com água pura no preparo do suco, ao invés de 1 litro conforme indica a embalagem, o mesmo teria concentração duas vezes maior do que o suco preparado corretamente.
- E) Ao retirar um copo de 200 mL desse 1 litro de suco, após ter si condições especificadas acima, o volume iria diminuir e consequentemente sua concentração iria aumentar.
A resposta correta é a letra C)
Questão 166

De acordo com os dados fornecidos pelo gráfico,
- A) a solubilidade do KNO₃ e do NaCl são iguais na temperatura de 38 ºC.
- B) a solubilidade do KNO₃ é maior que a do NaCl em qualquer temperatura.
- C) a 10 ºC é possível dissolver completamente 50 g de NaCl em 100 g de água.
- D) a 80 ºC é possível dissolver completamente 15 g de KNO₃ em 10 g de água.
A resposta correta é a letra D)
Em 80° a solubilidade é aproximadamente 160g/cm³. Assim,
160/10 = 16 cm³.
Portanto, qualquer valor abaixo de 16 cm³ será totalmente dissolvido.
167) Foram preparados 200 mL de solução contendo 20g de sacarose dissolvidos a uma temperatura de 25ºC.
- A) saturado;
- B) supersaturado;
- C) saturado com corpo de fundo;
- D) insaturado;
- E) diluído com corpo de fundo;
A resposta correta é a letra D)
Como a solubilidade da sacarose é 20g/100mL = 0,2 g/mL.
Como o composto preparado é 20g/200mL = 0,1 g/mL.
Logo, o composto preparado é insaturado pois tem concentração menor do que 0,2 g/mL.
168) Dicromato de potássio é um sólido alaranjado utilizado na fabricação de tintas e corantes. Sua fórmula é K₂Cr₂O₇.
- A) covalente.
- B) iônica.
- C) metálica.
- D) molecular.
- E) simples
A resposta correta é a letra B)
Questão 169

Observe as figuras abaixo.
Agora, marque a alternativa correta:
- A) Na figura I o líquido menos denso é o que está em baixo.
- B) Na figura II a bola de bilhar não afunda no mercúrio líquido devido sua densidade ser menor do que a densidade do mercúrio líquido.
- C) Na figura I ambos líquidos terão a cada um.
- D) Na figura I o líquido que está por cima possuirá uma massa maior comparado com volumes iguais dos dois líquidos.
- E) Se uma bola de bilhar fosse constituída por mercúrio líquido ela teria menor massa do que a bola de bilhar da figura II.
A resposta correta é a letra B)
Questão 170
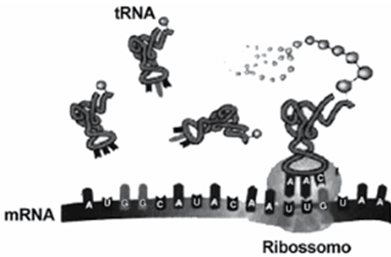
Esse processo resulta na
- A) absorção de aminoácidos.
- B) degradação de RNA.
- C) duplicação de DNA.
- D) formação de ribossomos.
- E) produção de proteínas.
A resposta correta é a letra E)
