Continua após a publicidade..
Proust verificou que as massas dos reagentes e as massas dos produtos que participam da reação obedecem sempre a uma proporção constante. Essa proporção é característica de cada reação, isto é, independe da quantidade de reagentes utilizados. Exemplo queima do carvão:
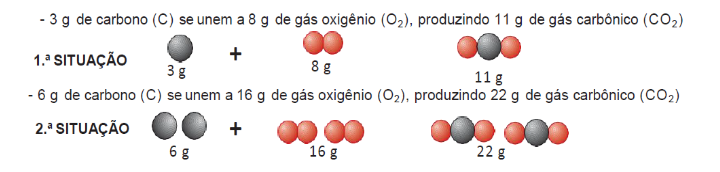
Observe a figura da 1ᵃ situação acima, do exemplo da queima do carvão, e identifique
- A) Reagentes:_______________
- B) Produtos: _______________
- C) Nº. de átomos dos reagentes _____ Nº. de átomos dos produtos _____
- D) Equação química:_______________________
- E) Podemos dizer que a Lei da Conservação de Massa foi observada? Justifique a sua resposta.
Resposta:
A) Reagentes: carbono C e oxigênio (O2)
B) Produtos: gás carbônico (CO2)
C) Nº. de átomos dos reagentes: 9 átomos de carbono e 24 átomos de oxigênio
Nº. de átomos dos produtos: 9 átomos de carbono e 24 átomos de oxigênio
D) Equação química: C + O2 -> CO2
E) Podemos dizer que a lei da conservação de massa foi observada, pois a soma das massas dos reagentes é igual à soma das massas dos produtos em ambas as situações. Isso significa que não houve perda ou ganho de matéria na reação, apenas uma transformação.

Deixe um comentário